Diskussion
Die vorliegend beobachteten Differenzen zwischen Ergebnissen bei einander entsprechenden Messungen der Basenabweichung sind in unterschiedlichem Ausma▀ prõanalytisch (z. B. Abnahmefehler, Lagerung oder BE-─nderungen durch das Verfahren der Tonometrie), intraanalytisch (z.B. mangelnde Stabilitõt oder Linearitõt der Elektroden, fehlerŁhafte Kalibration) und postanalytisch (z.B. Berechnungsmethode, Speicherung der Daten, RunŁdungsfehler) bedingt.
Quantitative Bewertung der Basenabweichung
Um die vorliegend beobachteten Schwankungen bei der Bestimmung der Basenabweichung in ihrer klinischen Relevanz einordnen zu k÷nnen, sollten die gefundenen Ergebnisse den in der Literatur berichteten Schwankungen gegen³bergestellt werden.
Dabei sollte jedoch auch ber³cksichtigt werden, da▀ das Konzept der Basenabweichung theoretisch und klinisch nicht v÷llig befriedigend ist, da die BE-Berechnung indirekt ³ber die PuffereigenŁschaften des Blutes (deren Konstanz oder zumindest Berechenbarkeit vorausgesetzt werden mu▀) erfolgt, ohne da▀ die darin enthaltenen Sõuren oder Basen selbst bestimmt werden. Bei Basendefizit ist eine m÷gliche Sõure das Laktat, das beispielsweise beim reinen hõmorrhagischen Schock vermutlich die gr÷▀te Bedeutung hat [DAVIS et al. 1994], allerdings bei anderen Formen der metabolischen Azidose nur eine untergeordnete Rolle spielt, wie die geringe Korrelation zwischen Laktatwerten und Basendefizit, BikarbonatŁkonzentration oder Anionenl³cke in einigen Studien gezeigt hat [DESHPANDE et al., 1997; Mikulaschek et al., 1996; ADUEN et al., 1995; VAN BIERVLIET et al., 1974]. Eine Identifizierung der zur BE-─nderung f³hrenden Substanz wõre jedoch in vielen Fõllen klinisch hilfreich, da St÷rungen des Sõure-Basen-Haushalts m÷glichst ursõchlich behandelt werden sollen. Trotzdem kann eine Abweichung des BE von den Erwartungswerten wichtige Hinweise auf Vorhandensein und Stõrke von Gesundheitsst÷rungen geben und in Verbindung mit anderen Befunden eine befriedigende Diagnose erm÷glichen.
Basenabweichung des Blutes (BEbl)
Referenzwerte f³r die Basenabweichung des Vollbluts (BEbl) wurden von M°ller (1959) und SIGGAARD-ANDERSEN (1963) ermittelt. Danach liegt das 95%-Konfidenzintervall f³r arterielles oder kapillares Blut beim erwachsenen Mann zwischen ¢2,4 und +2,2 bzw. ¢2,4 und + 2,3 mmol/L, f³r Frauen hingegen bei ¢3,3 bis +1,3 bzw. ¢3,3 bis +1,2 mmol/L. Angaben in Leitfõden, Handb³chern der Gerõte und Lehrb³chern variieren im Bereich ▒3 mmol/L. Aufgrund der Interdependenz der drei Parameter pH, pCO2 und BE wurden von HEKKING et al. (1995) multivariante Referenzregionen (ovale Bereiche in einem Stern aus drei Achsen f³r jeden der Parameter) vorgeschlagen, die einen interessanten neuen Ansatz zur Prõsentation von Laborwerten darstellen, mit etwas ▄bung eine Blickdiagnose ³ber den Sõure-Basen-Status und dessen Verlauf erm÷glichen, und deren Berechnung und Darstellung dank leistungsfõhiger Mikroprozessoren, hochaufl÷sender Bildschirme und Drucker, die bereits in die meisten Gerõte integriert sind, keinen wesentlichen Mehraufwand gegen³ber der blosen Zahlendarstellung mehr verursachen w³rde.
Unter bestimmten Bedingungen oder bei bestimmten Personengruppen wurden Verõnderungen des BEbl beobachtet. Hierzu geh÷rt unter anderem ein negativerer BEbl bei Kindern (z.B. ein um 2 mmol/L niedriger BEbl mit 2 bis 3 Jahren), nach Nahrungsaufnahme ein Anstieg um ca. 3 bis 4 mmol/L (insbesondere nach Gem³se) oder ein Abfall bei respiratorischer Alkalose als Zeichen von Kompensationsmechanismen. Als Extremwerte des BE des Blutes gelten ¢30 bis +30 mmol/L etwa unter Bedingungen des diabetischen Komas oder bei ausgeprõgtem Nierenversagen oder anhaltendem Erbrechen [SIGGAARD-ANDERSEN 1963].
RUTHERFORD und Kollegen (1992) f³hrten eine klinische Studie durch, um einen Zusammenhang zwischen einer negativen Basenabweichung (base deficit) und der Mortalitõt von Traumapatienten zu ermitteln. Die Patientendaten wurden nach Lebensalter, dem Vorliegen von Kopfverletzungen und von offenen Verletzungen in 8 Gruppen aufgeteilt. Beispielsweise bei Patienten ohne Kopfverletzungen, ohne offene Verletzungen und j³nger als 55 Jahre wurde bei einer Basenabweichung von ¢15 mmol/L eine Mortalitõt von 25 %, bei einer Basenabweichung von Ł22 mmol/L hingegen von 75 % beobachtet. Bei õlteren Patienten mit gleichem Verletzungsmuster fand dieser Mortalitõtsanstieg zwischen Ł11 und Ł17 mmol/L statt. Au▀er bei den Patienten, deren Mortalitõt auch bei ausgeglichenem Sõure-Basen-Haushalt aufgrund der Begleitverletzungen und des Alters schon ³ber 50 % lag, entsprach ein BE-Abfall von unter 5 mmol/L bereits einer Verdoppelung der Mortalitõt. Von MACKERSIE et al. (1989) wurde ein BE von unter ¢3 mmol/L bereits als bedeutendes Warnsignal f³r das vorliegen einer intraabdominellen Verletzung angesehen. Aus diesen Daten ist zu fordern, da▀ die Me▀genauigkeit des BE unter 3 mmol/L liegen sollte. Die Messungen der Studie von RUTHERFORD et al. (1992) wurden durch die Analysatoren AVL 995 und IL 1312 durchgef³hrt, deren Formeln nach Herstellerangabe bereits jenen der vorliegend untersuchten Nachfolgemodelle entsprachen. Somit unterscheiden sich die Basendefizite bereits rein rechnerisch (postanalytisch) um 1 bis 2 mmol/L (vgl. Abbildung 3). Nach den vorliegenden Ergebnissen ist auch eine intraanalytische Differenz zwischen den Gerõten bei der BE-Bestimmung wahrscheinlich. Da in der Mortalitõtsstudie von Rutherford nicht vermerkt ist, welche Messungen mit welchem der Gerõte durchgef³hrt wurden, ist eine ▄bertragung der Befunde auf Me▀ergebnisse in der klinischen Routine mit erheblichen Fehlerm÷glichkeiten behaftet. Auch in Tierversuchen an Schweinen [DAVIS et al. 1991 und 1994] konnte gezeigt werden, da▀ ein vorsõtzlich herbeigef³hrter hõmorrhagischer Schock den BE signifikant um etwa 10 mmol/L fallen lõ▀t. Dabei wurden BE-Werte im Schock von minimal nur ¢4,6 mmol/L erreicht.
Die gesunden Probanden der vorliegenden Untersuchungen hatten BEbl-Werte von ¢0,5 bzw. +1,2 mmol/L bei einheitlicher Berechnung aus den mittleren ven÷sen pCO2- und pH-Werten nach Gleichung 6 [ZANDER 1995]. Allerdings wurden vom Gerõt Nova Stat Profile Ultra in beiden Fõllen Werte von unter ¢5 mmol/L gemessen.
Basenabweichung unter Ber³cksichtigung der Extrazellulõrfl³ssigkeit (BEecf)
Untersuchungen zu Referenzwerten des BEecf liegen nicht vor. Es sollte jedoch wie beim BEbl von einem Normalwert von 0 mmol/L ausgegangen werden k÷nnen, da es sich definitionsgemõ▀ um eine Abweichung vom Normalwert handelt. Es werden unterschiedliche Intervalle im BereichĀ von ▒ 3 mmol/L angegeben. In dem von Radiometer verlegten Blutgas Handbuch wird ein Wert von ¢1,5 bis + 3 mmol/L f³r Mõnner und von ¢3,0 bis +2,0 mmol/L f³r Frauen angegeben. Sowohl IL als auch Nova Biomedical geben keinen Referenzbereich f³r den BEecf an. Prinzipiell erscheint eine ▄bertragung der Normalwerte vom BEbl auf den BEecf zulõssig, da sich die beiden Werte bei normalen pH- und pCO2-Werten fast nicht unterscheiden (vgl. Abbildung 2). Bei pathologischen Werten ist jedoch zu ber³cksichtigen, da▀ die BEecf-Werte bei Hyperkapnie oder Azidose ³ber den BEbl-Werten liegen, bei Hypokapnie und Alkalose hingegen darunter (vgl. Kapitel 0). SIEGEL und Kollegen (1990) f³hrten eine Mortalitõtsstudie an Patienten nach stumpfem Polytrauma durch, in der auch der BEecf ber³cksichtigt wurde. Dabei zeigte sich der BEecf unter 15 Laborparametern als wichtigster Indikator f³r die Mortalitõtswahrscheinlichkeit. Jedoch lag der mittlere BEecf der ³berlebenden Patienten nur um 5 mmol/L h÷her als der mittlere BEecf der verstorbenen (¢5 bzw. ¢10 mmol/L). In dieser Studie fand eine Verdoppelung der Mortalitõt von 25 auf 50% zwischen einem BEecf von ¢6 und ¢12 mmol/L statt. Der BEecf wurde mit einer einheitlichen Formel berechnet; Angaben zu den verwendeten Analysatoren wurden hingegen nicht gemacht. Aus diesen Ergebnissen, die im wesentlichen mit den Resultaten von RUTHERFORD et al. (1992) ³bereinstimmen, ergibt sich, da▀ auch BEecf-Unterschiede von unter 3 mmol/L zuverlõssig feststellbar sein sollten.
Bei den 20 Patienten der vorliegenden Untersuchung, die sich in klinisch stabilem Zustand einer planmõ▀ig verlaufenden thoraxchirurgischen Operation unterzogen, wurden unter Anwendung von Ausschlu▀kriterien (vgl. Kapitel 7.2.3) BEecf-Werte zwischen ¢9,3 und +7,3 mmol/L von den Gerõten ausgegeben. Bei einheitlicher Berechnung (Gl. 6) ergaben sich BEecf-Werte zwischen ¢9,4 und +6,2 mmol/L. Wenn der BEecf aus dem Mittelwert aller pH und pCO2-Messungen einer Probe bestimmt wurde, so wies der Patient mit der ausgeprõgtesten metabolischen Azidose einen BEecf (nach Gleichung 6) von ¢7,4 mmol/L und der Patient mit dem h÷chsten BEecf einen solchen von 2,9 mmol/L auf. Dies zeigt, da▀ Werte, die f³r das Vorliegen einer Alkalose sprechen w³rden, nur durch Me▀wertstreuungen und postanalytische Berechnungsunterschiede bedingt waren, und da▀ die Angabe von äNormalwertenō erheblich von der Berechnungsmethode abhõngt.
Offenbar ist weder aus der Literatur noch aus vorliegenden Ergebnissen eine Grenze bestimmbar, bis zu welchem Wert ein BEecf als physiologisch angesehen werden kann, wobei die Datenlage f³r metabolische Alkalosen noch unbefriedigender ist als f³r Azidosen.
Unterschiede der Berechnungsmethoden
Postanalytische Unterschiede in der Berechnung haben den Vorteil, da▀ sie prõzise reproduzierbar sind. Trotzdem k÷nnen sie, insbesondere wenn in einer Klinik verschiedene Berechnungsmethoden verwendet werden, praktische Bedeutung haben.
Basenabweichung des Blutes (BEbl)
Bei definitionsgemõ▀ normalem Sõure-Basen-Status (pH = 7,4; pCO2 = 40 mmHg, cHb = 15 g/dL) errechnen sich BEbl-Werte zwischen ¢0,5 (NCCLS und Ciba-Corning) und +0,8 mmol/L (Nova und IL), was etwa einem Drittel der Spannweite ³blicher Referenzbereiche entspricht (z. B. ¢1,5 bis 3 mmol/L). Da die BEbl-Formeln auch die Hõmoglobinkonzentration unterschiedlich ber³cksichtigen (vgl. Konstanten K2 und K4, ĀTab. 1), kommt es zu einer Verstõrkung dieses Unterschiedes bei anõmischen Patienten, so da▀ beispielsweise ein Patient mit einer cHb von 3 mmol/L und ansonsten normalem Sõure-Basen-Status gemõ▀ der vom NCCLS vorgeschlagenen Berechnungsmethode einen BEbl von ¢0,55 mmol/L aufweist, wohingegen sich nach der von Nova und IL verwendeten Formel ein BEbl von +0,96 mmol/L ergibt. Bei pH 7,36 w³rde der anõmische, normokapnische Patient nach der Berechnungsmethode des NCCLS bereits als metabolisch azidotisch eingestuft werden (BEbl = ¢3,06 mmol/L), hingegen w³rden die Gerõte von IL und Nova noch einen Wert ausgeben, der unauffõllig ist (BEbl = ¢1,60 mmol/L).
Besonders gro▀e Differenzen des BEbl treten bei teilkompensierten metabolischen Alkalosen zwischen der von Radiometer verwendeten Formel und den anderen Berechnungsmethoden auf. Beispielsweise errechnet sich bei pH = 7,65 und pCO2 = 50 mmHg eine BEbl-Differenz zwischen IL und Radiometer von 2,8 mmol/L (30,7 bzw. 27,9 mmol/L). Dies ist besonders bedenklich, da der Organismus gegen metabolische Alkalosen wesentlich weniger Kompensationsmechanismen besitzt als gegen Azidosen und Alkalosen durch LinksverŁschiebung der Sauerstoffbindungskurve die Sauerstoffversorgung des Organismus zusõtzlich st÷ren k÷nnen [SEELING et al., 1988].
Basenabweichung unter Ber³cksichtigung der Extrazellulõrfl³ssigkeit (BEecf)
Im Bereich der Normalwerte f³r pH und pCO2 betrõgt der maximale Unterschied der BEecf-Berechnungsergebnisse der Analysatoren 0,7 mmol/L (vgl. Abbildung 4), also etwa die Hõlfte der Differenz der BEbl-Werte (vgl. Abb. 3 und 4). Bei Abweichungen von den Normalwerten werden jedoch auch die Unterschiede zwischen den Formeln gr÷▀er. Bemerkenswert ist, da▀ die Formeln auf Basis des BEbl (Radiometer, ZANDER 1995) bei starken metabolischen Azidosen und insbesondere bei metabolischen Alkalosen das Ausma▀ der St÷rung im Vergleich zu den Formeln, die von Ciba-Corning und dem NCCLS [DEGEN et al., 1996] sowie von IL und Nova verwendet werden, deutlich geringer quantifizieren. Der Berechnungsvorschlag der IFCC [BURNETT 1995] liegt zumeist bei metabolischen Azidosen im Gerõtevergleich zwischen diesen beiden Gruppen, bei positiven Basenabweichungen ergeben sich jedoch Werte, die nahe bei den Ergebnissen des NCCLS-Vorschlags liegen (vgl. Abbildung 4).
Im Unterschied zum BEbl weicht im Vergleich zur modifizierten Formel nach ZANDER (Gleichung 6) bei teilkompensierten Alkalosen nicht nur die von Radiometer verwendete BEecf-Berechnungsmethode zunehmend nach unten ab, sondern zusõtzlich differieren die Algorithmen von IL, Nova, Ciba-Corning, dem NCCLS und dem IFCC in etwa gleichem Ma▀e in die entgegengesetzte Richtung. So betrõgt bei pH = 7,65 und pCO2 = 50 mmHg die BEecf-Differenz zwischen IL und Radiometer 4,6 mmol/L (34,6 bzw. 30,0 mmol/L).
Die im AVL Compact 2 errechneten Werte korrelieren mit den nach Gleichung 6 errechneten eng. Die Differenz betrõgt bei pH 7,6 maximal 0,4 mmol/L, bei pH 7,8 maximal 0,6 mmol/L. Im Bereich von pH 7,0 bis pH 7,4 liegen die Ergebnisse der beiden Formeln maximal 0,3 mmol/L auseinander. Wie weiter unten gezeigt (vgl. Tabelle), liegt dies an einer weitgehenden ▄bereinstimmung der Konstanten. Die Gefahr der niedrigeren BEecf-Werte bei den Gerõten von Radiometer und AVL, und auch bei Verwendung der Referenzformel nach Gleichung 6 besteht jedoch darin, da▀ ein Arzt, der andere BEecf-Berechnungsarten gewohnt ist, dadurch das Ausma▀ einer St÷rung unterschõtzen kann.
Bikarbonat
Die relative Abweichung zwischen den Faktoren von AVL und IL (ebenso wie Nova) betrõgt konŁstant ca. vier Prozent, was zu einer gleich gro▀en Abweichung bei allen berechneten BikarŁboŁnatŁwerten f³hrt. Bei den physiologischen Normalwerten pH = 7,4 und pCO2 = 40 mmHg erŁrechŁnen sich Bikarbonatkonzentrationen von 24,04 mmol/L (AVL) bzw. 25,01 mmol/L (IL / Nova).
Durch die pH-Abhõngigkeit des von Radiometer verwendeten Faktors zur Errechnung des Bikarbonats zeigen sich die Abweichungen dieser Berechnungsmethode insbesondere bei ausgeprõgten Azidosen und Alkalosen. Bei pH 7,0 betrõgt der Unterschied zwischen einem nach Radiometer und nach IL bzw. Nova berechneten Bikarbonat 6,1 % ; bei einem pCO2 von 80 mmHg ergibt dies 18,76 statt 19,91 mmol/L. Der Unterschied zwischen AVL und Radiometer betrõgt bei pH 7,8 etwa 8,2 %. Damit ergibt sich beispielsweise bei pH = 7,8 und pCO2 = 20 mmHg ein Bikarbonat von 30,2 statt 32,7 mmol/L. Trotz des geringf³gig h÷heren Rechenaufwands sollte die vonĀ SIGGAARD-ANDERSEN und ENGEL (1960) vorgeŁschlagene und von Radiometer verwendete etwas komplexeren Berechnungsmethode (vgl. Gl. 3) bevorzugt werden, da sie eher die tatsõchliche Bikarbonatkonzentration bestimmt und dabei kombinierte St÷rungen des Sõure-Basen-Haushaltes deutlicher werden (also Bikarbonatwerte bei Azidose niedriger und bei Alkalose h÷her angegeben werden).
Der Referenzbereich f³r Bikarbonat wird zumeist mit 22 bis 26 mmol/L angegeben. Jedoch zeigte sich vorliegend bei der ▄berpr³fung der Berechnungsmethoden, da▀ bei Normalwerten von pH (7,4) und pCO2 (40 mmHg) bereits Unterschiede von 1 mmol/L alleine durch Unterschiede in der Berechnung bedingt sind. So wird im IL 1620 OperatorÆs Manual (1996, S. 10-15) zwar als Normalwert (Mittelwert der oberen und unteren Grenze des Referenzbereiches) wie ³blich f³r pH 7,4 und f³r pCO2 40 mmHg angegeben, dies ergibt jedoch nach der in diesem Gerõt programmierten Formel eine Bikarbonatkonzentration (25,01 mmol/L), die bereits im oberen Viertel des auf derselben Seite angegebenen HCO3¢-Referenzbereiches liegt (22 bis 26 mmol/L). Bei Verwendung der gleichen BerechnungsŁmethode f³r das Bikarbonat schlõgt Nova Biomedical hingegen den etwas breiteren und im Mittel 0,5 mmol/L h÷heren Referenzbereich von 21 bis 28 mmol/L vor (Nova User Manual, Appendix D), so da▀ der aus pCO2 = 40 mmHg und pH = 7,4 errechnete Normalwert von 25,01 mmol/L dem Mittelwert des Referenzbereiches (24,5 mmol/L) nõher kommt und gleichzeitig der Abstand zur oberen Intervallgrenze gr÷▀er ist.
Die aktuell vorgeschlagenen Konstanten der IFCC und des NCCLS (siehe Tabelle 3) liegen sehr nahe beieinander (Differenz ca. 0,1%; cHCO3¢ = 24,2 mmol/L bei pCO2 = 40 mmHg und pH = 7,4), so da▀ sie praktisch gegeneinander austauschbar sind. Auch die Berechnung nach Radiometer unterscheidet sich bei normalem pH kaum davon (0,3% bzw. 0,2% bei pH 7,4; vgl. Abbildung 5).
Die von AVL verwendete Berechnungsmethode hat den Vorteil, da▀ sie bei pCO2 = 40 mmHg und pH = 7,4 ein Bikarbonat von 24,0 mmol/L ergibt, was der verbreitetste Normalwert ist [M▄LLER-PLATHE, 1982]. Dieser Normalwert wurde vor Einf³hrung der CO2-Elektrode mit einem Titrationsverfahren ermittelt. Obwohl gerade von Gegnern des BE-Konzepts [SCHWARTZ, RELMAN 1963] angef³hrt wird, da▀ es sich beim Bikarbonat um eine tatsõchlicheĀ Konzentration einer Substanz handle, ist dies aufgrund der heute ³blichen Berechnung aus pH und pCO2 nicht mehr zutreffend. Das Bikarbonat ist gegenwõrtig genau wie die Basenabweichung eine Gr÷▀e, die unter Annahme der Konstanz mehrerer Eigenschaften des Blutes errechnet wird. Zu beiden Parametern existieren titrimetrische bzw. tonometrische Me▀verfahren, die zwar nur noch selten angewendet werden, aber die M÷glichkeit bieten, die Berechnung der Bikarbonatkonzentration zu ³berpr³fen. Von FLEAR et al. (1987) wurden f³r den auf pH 7,4 justierten [RISPENS et al., 1968] Gleichgewichtskoeffizienten pK1', der gemeinsam mit dem L÷slichkeitskoeffizient s zur Berechnung der Bikarbonatkonzentration nach der Henderson-Hasselbalch-Gleichung verwendet wird, Werte zwischen 5,840 und 6,298 aus je sechs Messungen an Proben von gesunden Probanden und Patienten ermittelt. Dies entspricht einer interindivduellen m÷glichen Abweichung der realen Bikarbonatkonzentrationen bei gleichem pH und pCO2 von 7,8 %, wobei die Spanne bei gesunden Probanden sogar etwas gr÷▀er war als bei schwerkranken Patienten (jeweils n = 31).
Berechnung der Sauerstoffsõttigung
Die Gerõte ABL 510 (Radiometer) und Nova Stat Profile Ultra (Nova Biomedical) bestimmen die Sauerstoffsõttigung photometrisch, die anderen Gerõte errechnen diese mit unterschiedlichen Formeln aus dem pH, dem pO2 und teilweise aus dem pCO2. Die tatsõchlich verwendeten Formeln unterscheiden sich von der vorliegend verwendeten einheitlichen Formel (Gl. 7 und 8) um bis zu 2,4 % im Wertebereich der betrachteten Messungen, wobei die durchschnittlichen Differenzen mindestens um den Faktor 5 darunter liegen (vgl. Tabelle 13). Durch Einsetzen der unterschiedlich errechneten Sauerstoffsõttigungen in Gleichung 6 ergibt sich ein maximaler BE-Unterschied von 0,096 mmol/L. Diese Unterschiede wurden bei der Berechnung der Sauerstoffsõttigung f³r vorliegende Untersuchungen als nicht relevant angesehen.
Aus Gr³nden der Vergleichbarkeit zwischen den Gerõten wurden vorliegend nur aus dem Sauerstoffpartialdruck errechnete O2-Sõttigungen zur BE-Berechnung verwendet. Obwohl sich in diesen Messungen eine ³berraschend gute ▄bereinstimmung zwischen den photometrisch bestimmten und den errechneten Sauerstoffsõttigungen zeigte (vgl. Tabelle 13), ist das photometrische Verfahren im klinischen Einsatz jedoch prinzipiell vorzuziehen, insbesondere da es durch Messung bei verschiedenen Wellenlõngen die Unterscheidung zwischen verschiedenen Hõmoglobinarten erlaubt (z.B. Desoxyhõmoglobin, Hõmiglobin, CO-Hb, fetales Hb), wõhrend bei der Berechnung aus dem pO2 nur die partielle Sauerstoffsõttigung (Verhõltnis von oxygeniertem zu desoxygeniertem plus oxygeniertem Hõmoglobin) bestimmt werden kann, und damit in der klinischen Routine seltene, aber gravierende St÷rungen des Sauerstofftransports ³bersehen werden k÷nnen.
Auswirkung der Sauerstoffsõttigung auf den BE
Der Effekt des Korrekturterms f³r die Sauerstoffsõttigung (vgl. Gleichung 5) ist proportional zur Konzentration des desoxygenierten Hõmoglobins. Bei einer Sauerstoffsõttigung von 50 % und einer cHb von 20 g/dL (also 10 g Desoxyhõmoglobin pro dL) ergibt sich beispielsweise nach Gleichung 5 ein um 2 mmol/L niedrigerer BE. Der Zusammenhang, da▀ 10 g Desoxyhõmoglobin pro dL den BE um 2 mmol/L erh÷hen, kann vom behandelnden Arzt als Ausgangspunkt f³r ▄berschlagsrechnungen herangezogen werden.
BEbl im Vergleich gegen den BEecf
Die Basenabweichung des Vollblutes ber³cksichtigt nicht, da▀ jede Therapie auch das deutlich gr÷▀ere Volumen der interstitiellen Fl³ssigkeit beeinflu▀t. Daraus begr³ndet sich die Forderung, den äklassischenō BE in der klinischen Routine nicht mehr zu verwenden (SIGGAARD-ANDERSEN 1995, BURNETT 1995).
Wie aus Abbildung 2 ersichtlich ist, bewirkt die Betrachtung des BEbl anstelle des BEecf gerade bei den klinisch besonders relevanten Alkalosen mit Hyperkapnie eine Unterschõtzung der St÷rung, sofern der BEecf als BEbl bei niedriger Hõmoglobinkonzentration berechnet wird, wie bei der Referenzformel (Gleichung 6) und in den Gerõten von Radiometer und AVL der Fall (vgl. Tabelle). Bei Verwendung der NCCLS-Empfehlungen (Ciba-Corning, IL und Nova Biomedical), die sich nicht durch Einsetzen einer bestimmten Hõmoglobinkonzentration aus den BEbl-Konstanten errechnen lassen sind diese Unterschiede zwischen BEbl und BEecf sogar noch verstõrkt. BEecf-Werte sind bei diesen Analysatoren durch den Unterschied in der Konstanten K (vgl. Tabelle) primõr um ca. 7% gr÷▀er als entsprechende BEbl-Werte. Bei Azidose wird dieser Unterschied durch die h÷here Konstante becf kompensiert, bei Alkalose hingegen weiter verstõrkt. Dies bewirkt einen stõrkeren Anstieg des BEecf im Vergleich zum BEbl bei Hyperkapnie unter Verwendung der Algorithmen von IL, Nova und Ciba-Corning, der auch durch Vergleich der Abbildungen 3 und 4 feststellbar ist. Die im Vergleich zum BEbl h÷heren BEecf-Werte bei Hyperkapnie werden durch diese Berechnungsunterschiede noch verstõrkt, so da▀ beispielsweise bei einer vollstõndig kompensierten metabolischen Alkalose (pH = 7,4, pCO2 80 mmHg) der Unterschied zwischen BEbl und BEecf nach den BerechnungsŁmethoden von Ciba-Corning etwa 5 mmol/L betrõgt (BEbl = 18,7 bzw. BEecf = 23,6 mmol/L).
Tabelle 22: ĀĀĀ Konstanten zur Berechnung des BEbl bei konstanter Hõmoglobinkonzentration von 5 g/dL unter Verwendung der BEecf-Formel (Gleichung 2). Zum Vergleich sind die Konstanten, die von den Gerõten zur direkten BEecf-Berechnung verwendet oder vom IFCC empfohlen werden, (aus Tabelle 2) daneben dargestellt.
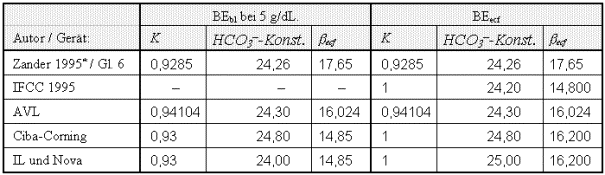
* Zu dieser Berechnungsmethode geh÷rt
eine Verminderung des BEbl bei unvollstõndiger
Ā Sauerstoffsõttigung (siehe Kapitel
3.1.1.4).
Die Gerõte von IL und Nova verwenden
dieselben Konstanten.
Die von Ciba-Corning verwendeten Konstanten entsprechen dem Vorschlag des NCCLS
(ehemals National Committee for Clinical
Laboratory Standards)[Degen et
al., 1996].
Es ist durchaus denkbar, da▀ bei vorliegen entsprechender klinischer Befunde aufgrund dieser nur durch die Betrachtung eines äanderen BEō bedingten Differenz die Entscheidung f³r oder gegen eine Argininhydrochlorid- bzw. Salzsõureinfusion gefõllt wird, die aufgrund ihres invasiven Charakters sehr vorsichtig und nur äals letzte Ma▀nahmeō durchgef³hrt werden sollte [SEELING, AHNEFELD 1988, S. 163].
Bei metabolischen Azidosen, die in der Therapie des hõmorrhagischen Schocks und des Polytraumas prognostisch und therapeutisch bedeutsam sind, liegen nach der Berechnungsmethode von ZANDER (1995) und AVL die BEbl-Werte tiefer als entsprechende BEecf-Werte (vgl. Abb. 1). Beispielsweise w³rde nach RUTHERFORD et al. (1992) eine Basenabweichung des Blutes von ¢18,6 mmol/L eine Mortalitõt von ³ber 50% bei j³ngeren Traumapatienten ohne Schõdelhirntrauma erwarten lassen. Mit dem Gerõt von AVL w³rde bei mõ▀iger Hyperkapnie (60 mmHg, pH 7,0) statt dieses BEbl jedoch ein BEecf von ¢15,4 mmol/L angegeben, der wiederum einer Mortalitõt von knapp 25 % entsprechen w³rde, wenn er mit diesen Mortalitõtsdaten verglichen w³rde. Bei pH = 7,0 und pCO2 = 80 mmHg ist der BEecf bei AVL sogar 4,0 mmol/L, bei Radiometer 4,1 mmol/L weniger negativ als der äklassischeō BEbl.
Dies verdeutlicht, da▀ mit der Umstellung von BEbl auf BEecf auch die Grenzwerte, von denen klinische Entscheidungen abhõngig gemacht werden, angepa▀t werden m³ssen. Solange nur wenige Studien vorliegen, die den BEecf verwenden, lõ▀t sich f³r eine ▄bergangsphase die zusõtzliche Angabe des äklassischenō BE trotz seiner theoretischen Redundanz rechtfertigen. Alle untersuchten Analysatoren geben beide Werte aus. Auch die international besetzte Consensus-Organisation NCCLS (ehemals National Committee for Clinical Laboratory Standards) empfiehlt weiterhin Algorithmen f³r beide Werte [DEGEN et al., 1996]. Eine weiterhin berechtigte Anwendung des BEbl sind in vitro Versuche, wie zum Beispiel die vorliegenden Tonometer-Me▀serien, die ihn aus methodischen Gr³nden erforderlich machen.
Gerõtespezifische Befunde zu den einzelnen BE-Formeln
AVL
Im Handbuch zum Analysator (Anhang S. 11-20) fand sich eine Formel f³r die Basenabweichung des Vollblutes, die deutlich andere Werte ergab als die Ausgabe des Gerõts.
Die nach R³ckfrage vom Hersteller zugesandte Formel f³r den BEbl ber³cksichtigte die O2-Sõttigung, wie bereits ³ber 2 Jahre zuvor angek³ndigt worden war [ZANDER 1995]. Allerdings gab es Abweichungen des BEbl bis zu 2,8 mmol/L, vor allem bei Proben mit geringen O2-Sõttigungen. Eine schriftlich detaillierte Darstellung der Diskrepanzen blieb trotz telefonischer R³ckfragen bis heute unbeantwortet. Eine genauere Betrachtung der Formel ergab jedoch, da▀ das Rechenzeichen vor dem Term zur Korrektur der O2-Sõttigung fõlschlich ein Pluszeichen war. Jedoch f³hrte auch die Korrektur nicht zur ▄bereinstimmung mit den Ausgaben des Gerõts. Erst das v÷llige Herausnehmen des Korrekturterms f³r die Sauerstoffsõttigung ergab eine ▄bereinstimmung. Die Formel im Originalhandbuch unterschied sich von der so erhaltenen nur durch ein fehlendes Klammerpaar. Also korrigiert AVL ebenso wie die anderen untersuchten Analysatoren den BE nicht in Abhõngigkeit von der Sauerstoffsõttigung.
Ciba-Corning
Die Formeln aus dem Anhang des OperatorÆs Manual f³r Bikarbonat, BEbl und BEecf stimmen mit Ausnahme von drei Messungen beim BEbl exakt mit der Gerõteausgabe ³berein. Es handelte sich in diesen drei Fõllen um Messungen, bei denen die cHb erst nach Ausdruck eines Me▀berichts eingegeben wurde. Der BEbl war in jedem Falle verõndert, aber nicht genau so, wie es aufgrund der angegebenen Formel zu erwarten wõre. Es liegt also vermutlich ein Rundungsfehler in der Abfrageroutine f³r bereits einmal ausgegebene Messungen vor. Obwohl durch diesen Fehler in der Programmierung der Abfrageroutine nur maximale Fehler von 0,2 mmol/L beobachtet wurden, zeigt diese Beobachtung beispielhaft, in welchen unerwarteten Situationen Programmierfehler in Laborgerõten zum Vorschein kommen k÷nnen.
Die exakte ▄bereinstimmung in den 392 anderen Fõllen ist dadurch erklõrbar, da▀ die Computereinheit zur Ein- und Ausgabe von Daten (User Interface Processor) offensichtlich mit einem Betriebssystem lõuft, dessen Flie▀kommaeinheit ebenfalls mit hoher Genauigkeit rechnet, und da▀ die Eingangsvariablen (pH, pCO2) gerundet (pH mit drei, pCO2 in mmHg mit einer Nachkommastelle) in die weiteren Berechnungen eingehen.
IL und Nova Biomedical
Die Nova-Gerõte das Gerõt IL 1620 verwenden dieselben Formeln, die den 1982 vom NCCLS (NCCLS PUBLICATIONS: Vol. 2 No. 10) vorgeschlagenen Formeln entsprechen. Jedoch werden vom NCCLS mittlerweile [DEGEN et al., 1996] andere KonŁstanten vorgeschlagen. Die õlteren NCCLS-Empfehlungen unterscheiden sich in vielen Fõllen erheblich von allen anderen vorliegend untersuchten Formeln, wobei sich in den meisten Wertebereichen vergleichsweise hohe Werte f³r die Parameter cHCO3¢, BEbl und BEecf errechnen (vgl. Abbildungen 3 bis 5). Es erscheint also ratsam, die Gerõte auf aktuelle Algorithmen umzustellen, wobei die Benutzer ³ber diese ─nderung informiert werden sollten.
Radiometer
Die Berechungsmethoden von Radiometer sind deutlich komplexer als die der anderen Hersteller. Dies erschwerte die Programmierung der Routine zur externen Berechnung. Die Formeln verwenden nur SI-Einheiten. Trotz der gro▀en Zahl an Zwischenschritten in der Berechnung stimmten die Rechenergebnisse und Gerõteausgaben gut ³berein. Dies zeigt, da▀ im Gerõt von Radiometer ebenfalls eine Recheneinheit mit hoher Prõzision verwendet wird. Die Verwendung der komplexen Formel wird damit begr³ndet, da▀ es insbesondere im Bereich hoher Hb-Konzentrationen Diskrepanzen zwischen der den anderen BEbl-Formeln zugrundeliegenden Van-Slyke-Gleichung und dem durch Titration ermittelten Nomogramm von SIGGAARD-ANDERSEN und ENGEL (1960) gebe, z.B. von 2,7 mmol/L bei der ung³nstigen Kombination aus cHb = 25 g/dl, BE = 10 mmol/L und pCO2 = 80 mmHg [CHRISTIANSEN, 1981]. Zwischen der von Radiometer verwendeten Formel und den anderen hier betrachteten BEecf-Formeln ist der maximale Unterschied bei einem BEbl von 10 mmol/L und pCO2 = 80 mmHg jedoch mit 2,1 mmol/L (IL bzw. Nova: 12,1 mmol/L) etwas geringer. Da noch nicht abschlie▀end geklõrt ist, was bei metabolischer Alkalose der äwahre in vivoō BE ist, kann als Gefahr der von Radiometer gewõhlten und den in vitro Messungen genauer entsprechenden Berechnungsmethode nur angef³hrt werden, da▀ ein Arzt, der Berechnungergebnisse der anderen Formeln gewohnt ist, das Ausma▀ einer metabolischen Alkalose unterschõtzen k÷nnte.
Praktischer Teil
Unterschiede zwischen Gerõteausgabe und externer Berechnung
Der geringe Unterschied zwischen den Gerõteausgaben und den berechneten Werten bei den errechneten Ma▀zahlen des Sõure-Basen-Status (Tabellen 10 bis 12) mu▀ nicht notwendigerweise auf eine Ungenauigkeit in der Formel zur³ckzuf³hren sein. Es ist auch denkbar, da▀ die Me▀werte mit h÷herer Genauigkeit oder mit anderen Einheiten in die Berechnungen einflie▀en, als sie ausgegeben werden. Beispielsweise k÷nnte der pCO2 mit 2 Nachkommastellen in der Einheit Kilopascal ber³cksichtigt werden, obwohl er mit nur einer Nachkommastelle in der Einheit mmHg ausgegeben wird, was zu geringf³gig valideren Ausgabewerten bei gerõteinterner Berechnung f³hren w³rde. Die im Mittel maximal 0,10 mmol/L und im Extremfall maximal 0,22 mmol/L gro▀en Differenzen wurden als tolerable Rundungsfehler betrachtet, so da▀ vorliegend alle BEbl-Werte extern berechnet wurden, um die bei den Tonometermessungen nur von zwei Gerõten bestimmten Hõmoglobinkonzentrationen bei allen Gerõten einheitlich zu ber³cksichtigen.
Wiederholungsgenauigkeit der Analysatoren
Aus Tabelle 14 ist ersichtlich, da▀ das Gerõt Nova Stat Profile 9 (Me▀reihen 1-10) die geringste Wiederholungsgenauigkeit aufwies. Die Stabilitõt des BEecf ist arteriell und ven÷s etwa gleich (in Tabelle 14 wird zwischen den beiden Probenarten nicht unterschieden).
Der Analysator von AVL streute in Serie 2 (Patienten 11 - 20) deutlich mehr, was ³berŁwiegend auf die pCO2-Messung zur³ckzuf³hren war (vgl. Tab. 14); aber auch die Wiederholungsgenauigkeit der pH-Messung nahm deutlich ab. Dieses Gerõt wies in der ersten Me▀serie von 10 Patienten die beste Wiederholungsgenauigkeit auf, in der zweiten Serie jedoch die schlechteste (sowohl bei den arteriellen als auch bei den ven÷sen Messungen). Allerdings hatte es auch in der zweiten Me▀serie bei nur 5 von 20 Proben die h÷chste Streuung der Me▀werte. Es fand sich keine kontinuierliche Verschlechterung der Prõzision innerhalb der zweiten Me▀serie; zum Beispiel wurden die ven÷sen Proben des 13. und des 18. Patienten durch das Gerõt von AVL am stabilsten gemessen. Aus Tabelle 14 geht ebenfalls hervor, da▀ die BE-Schwankungen des Nova Stat Profile 9 vor allem auf eine Instabilitõt der pCO2-Elektrode zur³ckzuf³hren waren (Standardfehler 2,70 mmHg). Auch die pH-Messungen waren im Vergleich zu den anderen Gerõten am wenigsten stabil (Standardfehler 0,0095), allerdings mit geringem Abstand zum Gerõt Ciba-Corning 860 (Standardfehler 0,0092).
Die zwischen den Serien mit Patientenblut nicht ausgetauschten drei Analysatoren haben alle in der ersten Serie sowohl arteriell als auch ven÷s geringere Streuungen der pCO2-Me▀werte aufgewiesen als in der zweiten Serie (vgl. Tabelle 14). Dies macht das Auftreten von Alterungsprozessen wahrscheinlich. Bei den Analysatoren von IL und AVL wurden direkt vor den Me▀serien und dreimal in der Zeit zwischen den beiden Serien (101 Tage) die Membranen gewechselt, so da▀ die verringerte Prõzision nicht durch gealterte Membranen bedingt war, sondern eher ein Alterungsproze▀ der Elektroden selbst oder anderer Teile der Analysatoren vermutet werden mu▀. Die Elektroden von Ciba-Corning sind laut Hersteller wartungsfrei, jedoch kam es auch bei diesem Gerõt zu einer deutlichen Zunahme der pCO2-Streuung zwischen den Me▀serien. Die pH-Messung õnderte ihre Prõzision hingegen weniger, und beim Gerõt von Ciba-Corning trat sogar eine Verbesserung der Wiederholungsgenauigkeit ein.
Am Blut gesunder Probanden wurde der pH von allen Analysatoren mit geringerer Streuung bestimmt (mittlerer Variationskoeffizient 0,08 %) als an Patientenblut (mittlerer Variationskoeffizient der zweiten Serie 0,11 %). Bei der Bestimmung des pCO2 war dieser Unterschied geringer (1,9 % bzw. 2,1 %) und uneinheitlich (vgl. Tabelle 14).
Von HILL et al. (1973) wurden bei f³nf untersuchten Analysatoren Standardabweichungen des pH bei Doppelbestimmung von 0,04 bis 0,14 gefunden. Bei den pCO2-Messungen in Blut lagen die Standardabweichungen zwischen 2,445 und 5,704 mmHg. Dies zeigt, da▀ die beim Gerõt Nova Stat Profile 9 beobachtete vergleichsweise geringe Wiederholungstreue des pCO2 fr³her f³r die markt³blichen Gerõte typisch war. F³r die anderen Gerõte zeigt der Vergleich hingegen eine deutliche Besserung der Prõzision der automatischen Analysatoren in den letzten 25 Jahren. Mit halbautomatischen Gerõten und den damals neu entwickenten Mikroelektroden wurden allerdings von SIGGAARD-ANDERSEN, ASTRUP und Kollegen bereits 1960 Standardabweichungen bei der pH-Messung von 0,006 f³r natives und 0,004 f³r õquilibriertes Blut ermittelt, die in etwa den vorliegend ermittelten Streuungen bei modernen automatischen Analysatoren entsprechen. Die Ergebnisse an nativem Blut waren damals jedoch weniger konstant, was vorliegend nicht festgestellt werden konnte (vgl. Tabellen 20 und 21).
Verteilung der Abweichungen
Zur Bewertung der potentiellen klinischen Relevanz von Me▀fehlern ist es wichtig zu wissen, wie oft mit gravierenden Ausrei▀ern gerechnet werden mu▀, da diese im Gegensatz zu konstanten Differenzen zwischen Gerõten oder zu langsamen Driftbewegungen der Me▀werte nicht mit gelegentlichen Kontrollmessungen festgestellt werden k÷nnen. Besonders bei der Verlaufsbeobachtung von Patienten k÷nnen spontane Me▀fehler von wenigen mmol/L zu bedeutenden Fehleinschõtzungen f³hren.
Wird eine Abweichung von ³ber 2 mmol/L zum Mittelwert der Messungen an derselben Probe als Ausrei▀er definiert, so kam es insgesamt zu 36 Ausrei▀ern, wovon 32 durch das Gerõt Nova Stat Profile 9 gemessen wurden (vgl. Tabelle) und auf Streuung des pCO2 zur³ckzuf³hren sind. Der gr÷▀te Ausrei▀er betrug 6,3 mmol/L. Von den verbleibenden vier Ausrei▀ern um mehr als 2 mmol/L stammen zwei Messungen mit um etwa 2,3 mmol/L erh÷hten BEecf-Werten vom Gerõt von IL und sind durch pH-Differenzen bedingt; die beiden verbleibenden Ausrei▀er waren durch vergleichsweise niedrige pCO2-Werte bedingt und wurden durch die Gerõte von AVL (3,3 mmol/L) und IL (2,3 mmol/L) verursacht.
Das Gerõt ABL 510 hatte die h÷chste Wiederholungsgenauigkeit und zeigte bei insgesamt 148 Messungen eine maximale Differenz von +0,66 bzw. ¢0,67 mmol/L zu den anderen Messungen an derselben Probe.
Die Ausrei▀er traten stets isoliert auf, wie aus einer Durchsicht der vorliegend nicht abgebildeten Boxplots hervorgeht. Die gr÷▀ten Abweichungen jedes Gerõts wurden einzeln gepr³ft, ohne da▀ sich Hinweise auf prõanalytische Fehler ergaben. Bei den Messungen des Gerõts Nova Stat Profile 9 fiel jedoch auf, da▀ extreme Ausrei▀er oft bei den ersten Messungen aus einer Spritze auftraten. Allerdings war Nova dabei nur in etwa einem F³nftel der Fõlle das erste Gerõt, dem die Probe zugef³hrt wurde, so da▀ auch hierbei nicht von einem prõanalytischen Fehler ausgegangen werden kann. Das Ansaugsystem der Nova-Gerõte ³ber eine Nadel lõ▀t auch eine Verõnderung des Blutes im Konusbereich nicht in Betracht kommen. Es ist eher zu vermuten, da▀ sich die pCO2-Elektrode erst wieder äeinmessenō mu▀te, um dann bei weiteren Messungen etwas prõzisere Werte zu liefern.
Tabelle 23:ĀĀĀĀĀ Verteilung der BE-Werte nach ihrer Differenz zum Mittelwert aller durch denselben Analysator an derselben Probe gemessenen Werte (vgl. Tab. 14). Die Intervalle f³r die BE-Differenzen sind in [mmol/L] angegeben; darunter findet sich die Anzahl der Messungen, deren BE-Wert minus dem BE-Mittelwert aller Messungen an derselben Probe im jeweiligen Intervall liegt. F³r die Messungen an Patientenblut wurde der BEecf errechnet, f³r die Messungen an Probandenblut hingegen der BEbl. Es wurden die jeweils gerõtespezifischen Formeln verwendet.
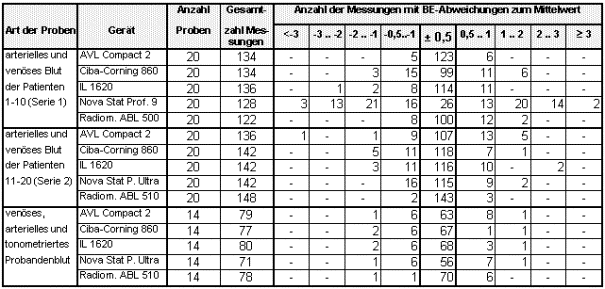
Die deutlich selteneren Ausrei▀er bei den Gerõten von Radiometer, insbesondere des ABL 510, und das Fehlen von Abweichungen von mehr als 1,2 mmol/L bei diesen Analysatoren ist vermutlich auf ein besseres Erkennen von Inhomogenitõten zur³ckzuf³hren. Es wurden auch Ergebnisse mit bis zu 3,7 mmol/L Differenz zum Durchschnitt der anderen Messungen von den Radiometer-Gerõten ausgegeben, allerdings waren die Me▀protokolle dabei immer mit einer entsprechenden Warnmeldung versehen, so da▀ die Messungen nicht ber³cksichtigt wurden.
Ausschlu▀ von Probenpaaren
F³r den Vergleich der Proben mit arteriellem und ven÷sem Blut ist von gro▀er Bedeutung, da▀ es sich tatsõchlich um f³r den Patienten reprõsentatives arterielles beziehungsweise ven÷ses Blut handelt. Bei 5 der Patienten zeigten sich signifikante Unterschiede zwischen Me▀parametern, bei denen keine oder nur sehr geringe Unterschiede zwischen arterieller und ven÷ser Messung zu erwarten sind und die keinen direkten Einflu▀ auf den BEecf haben. Eine m÷gliche Ursache f³r arterio-ven÷sen Differenzen k÷nnte in der Tatsache liegen, da▀ es sich bei den ven÷sen Proben um Blut aus der V. cava superior handelte, also nicht um gemischt ven÷ses, sondern nur um zentralven÷ses Blut. Bei dieser Entnahmeart ist nicht sicher vorhersagbar, aus welchem Teil des Blutkreislaufs das ven÷se Blut stammt, also welches Gewebe es zuletzt durchlaufen hat. Auf die entsprechende Problematik in Hinblick auf den Sauerstoffstatus wurde von BRANDT und MERTZLUFFT (1991) eingegangen. Bez³glich des Kohlendioxids ist von õhnlichen Effekten auszugehen. Allerdings ist bei der metabolischen Komponente des Sõure-Basen-Gleichgewichtes durch eine einmalige Kapillarpassage mit keinen starken ─nderungen zu rechnen, zumal die Organe, die in Ruhe die gr÷▀ten Mengen an nichtfl³chtigen Sõuren produzieren oder eliminieren k÷nnen (Leber mit Darm, Herzmuskel, Nieren) nicht in die Vena cava superior drainieren. Von ADROGU╔ et al. (1989) konnte eine gute ▄bereinstimmung der Blutgas- und pH-Werte zwischen zentralven÷sem und gemischtven÷sem Blut festgestellt werden, so da▀ die gemischtven÷se Entnahme f³r unn÷tig befunden wurde.
Die beobachteten Differenzen in der Hõmoglobinkonzentration von bis zu ³ber 50 % und die ausgeprõgten Elektrolytdifferenzen wõren durch eine unvollstõndige ven÷se Durchmischung nur erklõrbar, wenn die zentralven÷se Probe zu einem erheblichen Teil aus Infusionsl÷sungen bestanden hõtte, die wõhrend oder unmittelbar vor der Blutentnahme appliziert wurden und die sich noch nicht vollstõndig im zirkulierenden Blutvolumen verteilt hatten. Ebenso sind Verõnderungen durch Vermischung mit Resten von Infusionsl÷sungen oder von Antikoagulanzien, die zum Offenhalten des Katheters verwendet werden, m÷glich. Allerdings wurde vor Entnahme der zu analysierenden Spritzen jeweils eine Menge von 5 mL zum Verwerfen entnommen, so da▀ diese Fehlerquelle durch die angewandte Methodik ausgeschlossen war.Ā Die Ursache f³r die beobachteten Unterschiede der Zusammensetzung des arteriellen und ven÷sen Blutes konnte leider nicht geklõrt werden.
Kreuzvergleich der BE-Werte zwischen den Analysatoren
Die Differenzen zwischen den Analysatoren bei Messungen aus denselben Proben sind mit durchschnittlich bis zu 4,2 mmol/L (Ciba-Corning ¢1,41, Nova Stat Profile Ultra +2,83 mmol/L bei den Tonometermessungen, siehe Tab. 16) derart gro▀, da▀ damit in vielen Fõllen ohne Kenntnis des Analysators keine klinisch brauchbare Aussage m÷glich ist. Beispielsweise hatte ein Patient (Nr. 18) nach den Me▀ergebnissen durch das Gerõt Nova Stat Profile Ultra einen BEecf ven÷s von ¢1,8 mmol/L, nach den Messungen durch das Gerõt von Ciba-Corning jedoch eine gravierende Azidose von ¢6,4 mmol/L. Bei einem anderen Patienten (Nr. 17) war nach den Me▀ergebnissen des Analysators Nova Stat Profile Ultra von einer Alkalose auszugehen (BEecf = +6,0 mmol/L), jedoch gab das Gerõt Ciba-Corning 860 einen BEecf von 0,9 mmol/L an. Dabei handelte es sich jeweils um Mittelwerte aus 6 Messungen. Bei Einzelmessungen betrug der maximale Unterschied zwischen zwei Parallelmessungen aus derselben Probe 7,3 mmol/L (Ciba-Corning 860: 1,5 mmol/L, Nova Stat Profile 9: Ł5,8 mmol/L). Bei Ausschlu▀ der Messungen des Gerõts Nova Stat Profile 9 lag der maximale Unterschied bei 6,5 mmol/L (Nova Stat Profile Ultra: 7,3 mmol/L, Ciba-Corning 860: 0,8 mmol/L). Die Differenz zwischen den Gerõten ist offenbar gr÷▀er als die Gesamtbreite der ³blichen Referenzbereiche, so da▀ jede Blutprobe an mindestens einem der Analysatoren pathologische Werte aufweisen mu▀. In Anbetracht dieser Differenzen ist eine Festlegung von gerõteunabhõngigen Referenzwerten nicht m÷glich.
Wie aus Tabelle 16 ersichtlich, erh÷hten sich die Unterschiede zwischen den Analysatoren, die zwischen den Serien nicht ausgetauscht wurden, im zeitlichen Verlauf erheblich, z. B. zwischen Ciba-Corning 860 und AVL Compact 2 von 0,98 auf 4,17 mmol/L. Allerdings hatte in beiden Serien das Gerõt Ciba-Corning 860 die niedrigsten BE-Werte, mit statistisch signifikantem Abstand zum IL 1620, mit dem wiederum signifikant h÷here BE-Werte als mit dem AVL Compact 2 ermittelt wurden. Die Reihenfolge der nach dem gerõtespezifisch berechneten BE geordneten Gerõte õnderte sich also nicht. Auch die Reihenfolge der nach dem mittleren pCO2 sortierten Gerõte õndert sich nicht, jedoch sind die ausgetauschten Gerõte an jeweils anderer Position wie ihre Vorgõngermodelle (vgl. Tabelle Āa). Der Abstand zwischen dem Gerõt mit dem niedrigsten mittleren pCO2 (IL) und jenem mit dem h÷chsten pCO2 (AVL Compact 2) verringert sich sogar von 2,22 auf 1,53 mmHg. Bei den pH-Me▀ergebnissen drifteten die Analysatoren wõhrend der etwa 100 Tage zwischen den beiden Me▀serien mit Proben von Patienten hingegen stark auseinander (vgl. Tabelle Āb). Das Gerõt von AVL gab in Serie 1 um nur 0,0026 h÷here pH-Werte als Ciba-Corning aus, in Serie 2 betrug die Differenz hingegen 0,0359. Bei den 8 Tage vor Serie 2 durchgef³hrten Messungen an zum Teil tonometriertem Probandenblut war der Unterschied noch 0,0268.
Tabelle 24 a und b:
Darstellung der an allen Analysatoren parallel durchgef³hrten pCO2- (a) und pH-Messungen (b). Die Gerõte sind jeweils nach dem Mittelwert der Me▀werte geordnet. Als Ma▀ f³r die Streuung wurde die Standardabweichung der Differenz zwischen den jeweiligen Me▀werten und dem Mittelwert der Parallelmessungen errechnet. Versetzt zwischen den Zeilen der jeweiligen Analysatoren ist die Irrtumswahrscheinlichkeit p bez³glich der Ungleichheit der Verteilungen der Me▀werte (Wilcoxon Vorzeichen-Rang-Test) angegeben.
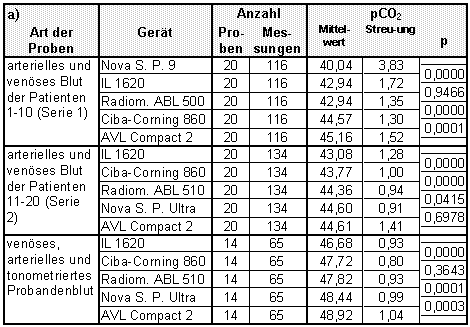
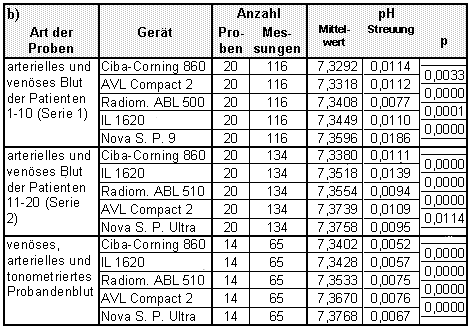
Der Abstand der pH-Mittelwerte zwischen dem Gerõt von Ciba-Corning und jenem von IL verringert sich hingegen sogar (von 0,0157 auf 0,0138 zwischen den Patientenserien bzw. auf 0,0026 zwischen der ersten Patientenserie und den Messungen mit Probandenblut; vgl. Tabelle Āb). Als naheliegende Ursache kõme daf³r in Betracht, da▀ sich der pH der Kalibrationspuffer, mit dem das Gerõt von AVL Kalibrationen durchf³hrte, entsprechend erniedrigte, dieser also saurer wurde. Eine m÷gliche Erklõrung daf³r wõre eine mikrobielle Kontamination.
Die Austauschgerõte nahmen bei der aufsteigenden Sortierung nach dem pH (vgl. Tabelle Āb) in beiden Fõllen die Position ihrer Vorgõngermodelle ein (Radiometer in mittlerer Position, Nova die h÷chsten pH-Werte), und auch die Differenz blieb fast konstant, was damit erklõrbar ist, da▀ die pH-Werte der Kalibrationspuffer und deren sonstige Zusammensetzung (äIonenstõrkeō) im wesentlichen gleich blieben.
Klinisch bedenklich ist, da▀ die Gerõte an denselben Proben den pH im Mittel um 0,0349 Einheiten unterschiedlich bestimmen, was ³ber die Hõlfte der Breite ³blicherweise angegebener Normalbereiche ist (z.B. pH 7,36 bis 7,42; vgl. LARSEN 1999).
Die kontinuierliche Zunahme der vom Gerõt AVL Compact 2 gemessenen pH-Werte im Vergleich zu den anderen Gerõten stellt einen deutlichen Hinweise daf³r dar, da▀ in diesem Fall relevante technische Probleme bez³glich der Langzeitkonstanz der zur Kalibration verwendeten Pufferl÷sungen bestanden.
─nderungen bei einheitlicher BEecf-Berechnung
Durch die einheitliche Berechnung nach dem Vorschlag von ZANDER (1995) ergab sich in der ersten Serie der Messungen mit Patientenblut etwa eine Halbierung der Differenz zwischen dem Gerõt mit den niedrigsten BEecf-Werten (Ciba-Corning 860) und jenem mit den h÷chsten (AVL Compact 2) von 1,02 auf 0,47 mmol/L (vgl. Tabelle 16). 3 Į Monate spõter bewirkte die einheitliche Berechnung nur noch eine Reduzierung der Differenz um ca. 20 % von 4,57 auf 3,70 mmol/L, was jedoch in diesem Falle 0,87 mmol/L entsprach.
Es zeigte sich also, da▀ die einheitliche BE-Berechnung bei gut kalibrierten Gerõten die VerŁgleichbarkeit zwischen den Me▀ergebnissen relevant verbessern kann, indem die Differenzen um mehr als die Hõlfte gesenkt werden. Wenn die Unterschiede in den Eingangsvariablen zur BE-Berechnung (z. B. aufgrund mangelhafter Kalibration) jedoch zuŁnehmen, tritt der Nutzen der einheitlichen Berechnung gegen³ber den Me▀unterschieden zwischen den Gerõten in den Hintergrund.
Kreuzvergleich der integrierten Barometer
In vorliegender Untersuchung ergab sich kein Hinweis daf³r, da▀ Ungenauigkeiten in der Luftdruckmessung zu relevanten Fehlern bei der BE-Bestimmung f³hrten. Die integrierten Barometer stimmten mit maximalen Abweichungen von 3,3 mmHg, was einem relativen Fehler bei der Bestimmung der Gaspartialdr³cke von unter 0,5 % entspricht, weitgehend ³berein. Die systematischen Unterschiede zwischen den Gerõten von bis zu 13 % bei der pCO2-Bestimmung (vgl. Tabelle 14) k÷nnen nicht wesentlich durch Unterschiede bei der Lufdruckmessung verursacht sein. Wesentliche Streuungen zwischen Messungen wurden nicht beobachtet, jedoch kam es wõhrend der Versuche zu ─nderungen um bis zu 2 mmHg gegen³ber dem Referenzbarometer innerhalb von 8 Tagen, die nachkorrigiert wurden. Eine Aussage ³ber die Langzeitkonstanz war nicht m÷glich.
Einflu▀ der Hõmoglobinkonzentration
Die Hõmoglobinkonzentration (cHb) wird von beiden Gerõten des Herstellers Nova Biomedical und dem ABL 510 (Radiometer) bestimmt. Sie eignet sich besonders, um Verd³nnungseffekte oder Fehler durch Sedimentation von Erythrozyten aufzudecken. In der ersten Serie der Messungen an Patientenblut wurde die cHb nur durch Nova Stat Profile 9 aus dem elektrischen Leitwert des Blutes errechnet. In der zweiten Hõlfte erfolgte die Bestimmung im Gerõt Nova Stat Profile Ultra durch Messung des Leitwerts mit Natriumkorrektur und im Analysator ABL 510 photometrisch.
Die Standardfehler der Hõmoglobinkonzentration bei Wiederholungsmessungen an derselben Probe waren derart gro▀, da▀ nur bei drei Patienten (Nummern 1, 13 und 14) statistisch signifikante Unterschiede zwischen der arteriellen und der ven÷sen Probe nachweisbar waren, obwohl sich die Mittelwerte auch bei anderen Probenpaaren um ³ber 10 % voneinander unterschieden (Nummern 2, 4, 9 und 12). Weder bei Nova noch bei Radiometer war durch Betrachtung der Einzelwerte erkennbar, aus welchen Gr³nden besonders starke Abweichungen auftraten. Zumeist waren starke Abweichungen so hõufig, da▀ sie im Boxplott nicht als Ausrei▀er ausgewiesen wurden, aber auch die ausgewiesenen Ausrei▀er sind recht gleichmõ▀ig ³ber die Me▀wiederholungen verteilt. Die durchschnittlichen Standardfehler zum Mittelwert der Wiederholungsmessungen betrugen 2,23 (Nova 9), 1,03 (Nova Ultra) und 1,38 (Radiometer) g/dL (Variationskoeffizienten 22,1, 9,5 bzw. 14,5 %).
F³r die blo▀e Berechnung des BEbl, der ja zumeist ohnehin klinisch weniger Bedeutung hat als der BEecf, mag diese geringe Prõzision (³ber 5 % der direkt aufeinanderfolgenden Messungen wichen um mehr als 2 g/dL voneinander ab) in aller Regel gen³gen. Eine Erh÷hung des cHb aller Proben der Patientenmessungen um 2 g/dL hõtte den mittleren BEbl von 2,09 auf Ł2,17 mmol/L gesenkt (Berechnung nach ZANDER 1995). Die BEbl-Berechnung mit einer cHb von konstant 15 g/dL bei allen Analysatoren hõtte statt dessen einen mittleren BEbl von Ł2,24 mmol/L ergeben. Insgesamt ist der Einflu▀ der cHb auf den BEbl au▀er bei starken Anõmien und gleichzeitig bestehenden starken Hyper- oder Hypokapnien recht gering (vgl. Abbildung 2). Eine ausgeprõgte Anõmie eines Patienten mu▀ aufgrund der geringen Wiederholungsgenauigkeit der Gerõte ohnehin auf andere Weise diagnostiziert und kontrolliert werden; in diesem Fall kann bei Vorhandensein einer Abnormitõt des pCO2 mit geringem Aufwand die Hõmoglobinkonzentration in die Analysatoren eingegeben werden, falls der Parameter BEbl trotz der Vorz³ge des BEecf berechnet werden soll.
Die cHb-Messungen an nativem und tonometriertem Blut gesunder Probanden wiesen nur einen Standardfehler von 0,26 (Radiometer) bzw. 0,33 g/dL (Nova Ultra) auf (Variationskoeffizienten 1,7 bzw. 2,3 % ). Bei Messungen von GOUGET et al. (1992) fand sich ein Variationskoeffizient von 1,6 %. Offenbar wird also die Hõmoglobinkonzentration ebenso wie der pH in Blut gesunder Probanden von den vorliegend untersuchten Gerõten mit einer wesentlich besseren Prõzision bestimmt als in Blut von Patienten wõhrend thoraxchirurgischer Operationen.
Vergleich zwischen arteriellen und ven÷sen Messungen
Statistische Verteilung der Differenzen
Die Verteilung der Differenzen aus arteriellen und ven÷sen Proben wich deutlich von der Normalverteilung ab (34 % Wahrscheinlichkeit nach Kolmogorow-Smirnow). Sofern nur Messungen ber³cksichtigt wurden, bei denen mindestens 6 g³ltige Messungen je Gerõt an beiden Proben eine Standardabweichung von < 0,4 mmol/L aufwiesen, f³hrte dies zu einer noch geringeren Wahrscheinlichkeit im Kolmogorow-Smirnow-Test von 8% mit einer W÷lbung von 3,942 (Standardfehler 0,330) und einer Schiefe von 0,978 (Standardfehler 0,166). Als Ursache daf³r zeigte die Datensichtung stark erh÷hte arterielle Me▀werte bei den Blutproben des sechsten der insgesamt 20 Patienten (Probenpaar 6) und erh÷hte ven÷se Werte bei den Probenpaaren 4 und 5. Der zusõtzliche Ausschlu▀ dieser Messungen f³hrt zu einer guten Normalverteilung der 196 verbleibenden arterio-ven÷sen Differenzen (SD 0,402; W÷lbung ¢0,370, SE 0,346; Schiefe 0,131, SE 0,174; p = 78%).
Bei den Probenpaaren 4, 5 und 6 ist also nach den BE-Me▀ergebnissen ebenfalls eine noch nicht vollstõndige Verteilung von Infusionsl÷sung oder ein Abnahmefehler plausibel, der sich jedoch im Gegensatz zu den Probenpaaren 1, 9, 12, 13 und 14 nicht durch Me▀parameter ohne direkten Bezug zum BEecf nachweisen lie▀. Allerdings lag beispielsweise bei Probenpaar 4 eine arterio-ven÷se cHb-Differenz von 24% und bei Probenpaar 5 eine Glukose-Differenz von 10% vor, die jedoch aufgrund der starken Streuung dieser Me▀werte im Wilcoxon Vorzeichen-Rang-Test nicht signifikant waren.
Wenn nur Messungen ber³cksichtigt wurden, bei denen mindestens 6 g³ltige Messungen je Gerõt an beiden Proben eine Standardabweichung von < 0,4 mmol/L aufweisen und nur die Probenpaare 2, 3, 7, 8, 10, 11, 15, 16, 17, 18, 19 und 20 eingeschlossen wurden, verringerte sich die Standardabweichungen der verbleibenden arterio-ven÷sen Differenzen von etwa 0,7 mmol/L auf 0,4 mmol/L (mit geringer Abhõngigkeit von der verwendeten Formel), aufgrund der geringeren Fallzahl (n = 205) blieb die Breite der Konfidenzintervalle f³r die arterio-ven÷se Korrelation jedoch praktisch unverõndert (0,113 statt 0,133 mmol/L [¢0,167; Ł0,034] bei der in der letzten Zeile von Tabelle 18 verwendeten Berechnungsart), und die dadurch bewirkte ─nderung der mittleren arterio-ven÷sen Differenzen betrug nur 0,017 mmol/L. Ebenso verbesserte sich R2 als Streuungsma▀ der linearen Regression von etwa 0,95 auf 0,97, jedoch gab es keine signifikanten ─nderungen der Regressionsgeraden.
Es lõ▀t sich also bei Anwendung dieser verschõrften Ausschlu▀kriterien eine deutlich bessere Annõherung der arterio-ven÷sen Differenzen an die Normalverteilung erreichen. Alle vorŁlieŁgenden statistischen Auswertungen wurden daher auch unter Ber³cksichtigung nur dieser 205 Messungen durchgef³hrt. Die Unterschiede zu den Ergebnissen, die sich bei Ber³cksichtigung der 468 Messungen nach den urspr³nglichen Ausschlu▀kriterien ergaben, sind jedoch gering und statistisch nicht signifikant, so da▀ sie im folgenden nicht dargestellt werden.
Korrelation zwischen arteriellen und ven÷sen Proben
Die Abbildung 6 zeigt, da▀ die ven÷se ▄berschõtzung des BEecf durch Ber³cksichtigung des Haldane-Effektes in der BEecf-Berechnung bis unter die ³bliche Anzeigegenauigkeit der Basenabweichugung von 0,1 mmol/L reduziert werden kann. Die Verwendung einer konstanten Hõmoglobinkonzentration von 15 g/dL zur BEecf-Berechnung ergibt dabei eine geringf³gig, aber statistisch signifikant bessere arterio-ven÷se ▄bereinstimmung als die Verwendung der gemessenen Hõmoglobinkonzentrationen von durchschnittlich 10,64 g/dL (vgl. Tabelle 18, letzte 2 Zeilen). Dies lõ▀t vermuten, da▀ der Haldane-Effekt noch nicht ausreichend stark ber³cksichtigt wurde. Erst wenn der zugeh÷rige Faktor um ╝ erh÷ht wird (von 0,2 auf 0,25, vgl. Gleichungen 5 und 6), wird der BEecf Unterschied zwischen den arteriellen und den ven÷sen Proben auf +0,003 ▒ 0,729 mmol/L reduziert.
Von Radiometer wird die formal komplexeste Formel verwendet, die, soweit bekannt, am genausten nach Referenzmessungen modelliert wurde. Wie allerdings aus Tabelle 18 ersichtlich ist, gen³gt bei dieser Formel der Korrekturterm nach Gleichung 5 ebenfalls nicht, um die Werte der ven÷sen Messungen ausreichend zu reduzieren. Bei dieser Formel ist, wenn die tatsõchlichen Hõmoglobinkonzentrationen eingesetzt werden und die cHbecf als 1/3 cHbProbe angeŁnommen wird, sogar eine Erh÷hung des Korrekturfaktors auf 0,3 notwendig, um die mittlere arterio-ven÷se Differenz praktisch vollstõndig zu eliminieren (+0,012 ▒ 0,724 mmol/L, 95%-Konfidenzintervall [-0,078; +0,053]).
Bereits PHILLIPS und PERETZ (1969) kamen zu dem Ergebnis, da▀ der BE zwischen arteriellen und gemischtven÷sen Proben eng korreliert. Der mittlere arterio-ven÷se BE- Unterschied aus 41 Messungen betrug dabei nur 0,28 mmol/L. Ein paralleler Verlauf des arteriellen und ven÷sen BE wurde auch ³ber den gesamten Verlauf des hõmorrhagischen Schocks bei Schweinen gefunden [DAVIS, 1994], wobei die ven÷sen Werte etwa 2,5 mmol/L tiefer als die arteriellen waren, was durch die fehlende sO2-Korrektur erklõrbar ist. Bei vorliegenden Messungen (vgl. Tabelle 18) ergab sich eine arterio-ven÷se BEecf-Differenz vor sO2-Korrektur von etwa 0,6 mmol/L. Diese niedrigere Differenz erklõrt sich dadurch, da▀ bei den vorliegend untersuchten kreislaufstabilen Patienten die mittlere ven÷se Sauerstoffsõttigung noch ³ber 79 % betrug, wõhrend sie bei den von DAVIS (1994) untersuchten Schweinen auf bis zu 43 % abfiel.
Bereits 1937 wurde der Haldane-Effekt im pH-Bereich von 7,0 - 7,8 als annõhernd konstant mit 0,03 mmol/L je Gramm Hõmoglobin angegeben [DILL et al., 1937], so da▀ auch SIGGAARD-ANDERSEN (1963) die Korrekturformel (vgl. Gl. 5) mit einem Faktor von 0,3 angab, was weitgehend mit den vorliegenden Ergebnissen ³bereinstimmt.
Zuverlõssigkeit von ven÷sen BE-Werten als Ersatz f³r arterielle BE-Messungen
In bestimmten klinischen Situationen kann es praktikabler sein, den BEecf aus vorhandenem oder leichter zu erhaltendem ven÷sem Blut anstelle von arteriellem zu bestimmen. Wie vorliegend gezeigt, lõ▀t sich die mittlere arterio-ven÷se Differenz durch entsprechende Ber³cksichtigung der Sauerstoffsõttigung bis weit unter die mit heutigen Gerõten zu erwartende Standardabweichung bei Me▀wiederholungen reduzieren. Um beurteilen zu k÷nnen, ob ven÷se BE-Messungen arterielle tatsõchlich ersetzen k÷nnen, ist es jedoch auch notwendig, die Verteilung der jeweiligen Me▀ergebnisse auf ▄bereinstimmung zu pr³fen. Zu diesem Zweck kann untersucht werden, ob eine ven÷se Messung genauso gut wie eine arterielle Messung der jeweils letzten arteriellen Messung entspricht. Die Ergebnisse dieser Pr³fungen sind in Tabelle dargestellt. Dort ist ersichtlich, da▀ der BE im Mittel zwischen zwei aufeinanderfolgenden arteriellen oder ven÷sen Messungen um 0,09 (bei Anwendung der strengeren Ausschlu▀kriterien aus Kapitel 0 um 0,04 mmol/L) abfiel, was unter anderem Folge der metabolischen Aktivitõt im Blut wõhrend der Zeit ohne K³hlung sein kann. Dieser BE-Abfall darf im arterio-ven÷sen Vergleich nicht erwartet werden, da gepaarte Messungen verglichen werden, bei denen die beiden Spritzen etwa gleich lange f³r gleich viele Messungen aus dem Eiswasserbad genommen worden waren. Zielwert der mittleren arterio-ven÷sen BE-Differenz ist daher 0.
Tabelle25: ĀĀĀĀĀ Gegen³berstellung der Mittelwerte der BEecf-Differenzen zwischen je einer Messung an Patientenblut und der folgenden Messung an derselben Probe sowie der BEecf-Differenzen zwischen den arteriellen und ven÷sen Paarmessungen. Es wurden nur die (n = 397) Messungen ber³cksichtigt, auf die direkt eine g³ltige arterielle Messung an derselben Probe und eine g³ltige ven÷se Messung an der simultan abgenommenen Probe folgte (die jeweils letzten Messungen beim arterio-ven÷sen Vergleich blieben unber³cksichtigt: äerste bis vorletzte Messungō).
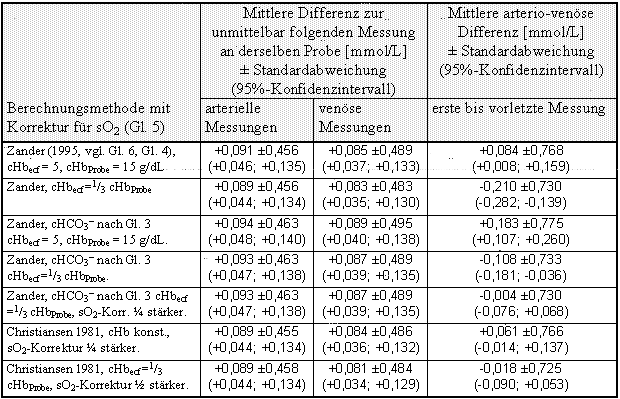
Bei 10 der 15 Probenpaare war die ven÷se Streuung gr÷▀er als die arterielle (im Mittel 6 %), was nach dem Wilcoxon Vorzeichen-Rang-Test mit p = 0,03 signifikant ist. Die Streuung zwischen einem arteriellen und einem zugeh÷rigen ven÷sen Me▀ergebnis war etwa 60 % gr÷▀er als die Streuung zwischen zwei aufeinanderfolgenden arteriellen Messungen. Die maximale arterio-ven÷se Differenz betrug bei den hier betrachteten 397 Messungen bei BEecf-Berechnung nach der Formel, die in der letzten Zeilen von Tabelle verwendet wird ¢2,54 bzw. +2,88 mmol/L, die maximale Differenz zwischen zwei aufeinanderfolgenden Messungen betrug ¢1,40 bzw. + 2,1 mmol/L.
Dies bedeutet, da▀ beim Ersatz einer arteriellen durch eine ven÷se Messung auch bei sO2-Korrektur mit einer Zunahme der Streuung des BEecf um etwa 60 % im Vergleich zur MehrfachŁbestimmung an derselben Probe gerechnet werden mu▀. Allerdings kann durch diesen Vergleich keine Aussage dar³ber gemacht werden, ob die Streuung bei gleichzeitiger arterieller Entnahme ³ber zwei Wege geringer wõre als bei gleichzeitiger arterieller und ven÷ser Entnahme. Ebenso darf nicht vorausgesetzt werden, da▀ arterielle BEecf-Werte eine gr÷▀ere klinische Aussagekraft haben als ven÷se.
Bei nicht kompensiertem Kreislauf- oder Lungenversagen oder Schock sollten in jedem Falle arterielle und ven÷sen Proben analysiert werden, da die arteriellen Blutgaswerte eher eine Aussage ³ber die Effizienz der Beatmung erm÷glichen, die ven÷sen hingegen eher ³ber den Verlauf der Folgen einer eventuellen Gewebehypoxie [WEIL et al., 1986].
Ven÷se und arterielle Kontrollmessungen bei gesunden Probanden
Bereits am frisch abgenommenen Blut zeigten sich erhebliche Unterschiede in den ven÷sen BE-Werten, die von den einzelnen Analysatoren bestimmt wurden.
Nach den Messungen des Gerõtes Nova Stat Profile Ultra des Analysators der Firma AVL hõtte man die subjektiv gesunden Probanden an beiden Tagen in einer Notaufnahme m÷glicherweise aufgrund einer vermeintlichen metabolischen Alkalose weitergehend untersucht oder sogar therapiert (vgl. Tabellen 20 und 21).
Der ven÷se CO2-Partialdruck war nach Angabe aller Gerõte in der zweiten Me▀serie etwa 10 mmHg niedriger als in der ersten Me▀serie. Es fõllt auf, da▀ die durchschnittlichen pCO2-Werte am ersten Tag deutlich ³ber den von SIGGAARD-ANDERSEN (1963) und M°ller (1959) angegebenen Referenzwerten mit 95% Konfidenzintervallen von 35,8 bis 46,6 mmol/L bzw. 39,3 bis 48,9 mmol/L liegen, auch wenn nachĀ M▄LLER-PLATHE (1982) und ADROGU╔ (1989) von einem um ca. 5 mmHg h÷heren pCO2 ausgegangen werden kann, da es sich um ven÷se Proben handelt. Auch die durchschnittliche ven÷se Sauerstoffsõttigung unterschied sich zwischen den beiden Tagen um 15,3 %. Die Blutabnahmen waren an Personen durchgef³hrt worden, die sich wõhrend mindestens 10 Minuten nicht bedeutsam k÷rperlich betõtigt hatten, ³ber normale k÷rperliche Leistungsfõhigkeit verf³gten und unter keiner Lungenkrankheit litten. Auch der pCO2 der ven÷sen Probe des zweiten Probanden lag noch ³ber dem oberen Referenzwert. Der veno-arterielle Unterschied betrug dabei ca. 10 mmHg. Bei den vorliegenden Messungen an Patientenblut ergab sich wõhrend Operationen eine durchŁschnittliche veno-arterielle Differenz von nur 3,6 mmHg. Eine m÷gliche Erklõrung f³r die gr÷▀ere Differenz bei den wachen, gesunden Probanden wõre ein unbewu▀te mõ▀ige Hyperventilation unmittelbar vor der Punktion der Femoralarterie, da diese verglichen mit einer ven÷sen Blutentnahme einen etwas invasiveren Charakter aufweist.
Im Mittel fiel der BEbl der ven÷sen Kontrolle bei einheitlicher Berechnung am ersten Me▀tag um 0,05 mmol/L (vgl. Tabelle 19) wõhrend mehr als 6 Stunden Lagerung. In der zweiten Me▀serie waren es 0,69 mmol/L bei der ven÷sen und 0,5 mmol/L bei der arteriellen Kontrollprobe in etwa 3 Stunden 15 Minuten. Der pCO2 stieg um maximal 1,24 mmHg an. Innerhalb der je 8 ven÷sen Anfangsmessungen wõhrend einer Zeitspanne von 44 (erste Me▀serie) bzw. 24 Minuten (zweite Me▀serie) fiel der BEbl hingegen um durchschnittlich 0,78 bzw. 0,70 mmol/L. Durch diesen Vergleich wird deutlich, da▀ kurze Zeiten, in denen das Blut nicht gek³hlt wird, einen bedeutend gr÷▀eren Einflu▀ auf den BE haben als mehrst³ndige Lagerungszeiten in Eiswasser.
Der BEbl der arteriellen Probe wurde nach den gerõtespezifischen Formeln vor den Messungen an tonometriertem Blut durchschnittlich um 1,78 mmol/L niedriger und nach ca. 3 ╝ Stunden Lagerung um 1,45 mmol/L niedriger als der ven÷se BEbl errechnet (vgl. Tabelle 19). Bei einheitlicher Berechnung unter Ber³cksichtigung der Sauerstoffsõttigung (Gleichung 6) betrug der Unterschied noch 0,45 bzw. 0,22 mmol/L. Durch Erh÷hung des Faktors im Korrekturterm (Gleichung 5) auf 0,3 [mmol/L pro 10 g Hõmoglobin] wird die arterio-ven÷se BEbl-Differenz sogar geringf³gig, jedoch nicht signifikant ³berkompensiert (vgl. Tabelle). Wird jedoch der BEecf statt des BEbl betrachtet, so erh÷ht sich die arterio-ven÷se Differenz (abhõngig von der Berechnungsmethode) um 0,5 bis 1 mmol/L. Dies ist dadurch bedingt, da▀ die BEecf-Berechnung (die prinzipiell der BEbl-Berechnung mit niedriger cHb entspricht) bei erh÷htem pCO2, also z. B. bei ven÷ser Messung, im Vergleich zur BEbl-Berechnung h÷here Werte ergibt (vgl. Abbildung 2). Bei diesen Messergebnissen w³rde erst ein Faktor von 0,4 die arterio-ven÷se Differenz des BEecf weitgehend beseitigen.
Tabelle26: ĀĀĀĀĀ BE-Differenzen zwischen arteriellen und ven÷sen Blutproben eines gesunden Probanden bei unterschiedlichen Methoden zur BE-Berechnung und verschieden starker sO2-Korrektur. Arterielle und ven÷se Proben wurden sowohl kurz nach Entnahme als auch am Ende der Me▀serie analysiert. Die nach dem t-Test f³r unverbundene Stichproben signifikanten Differenzen sind fett gedruckt.
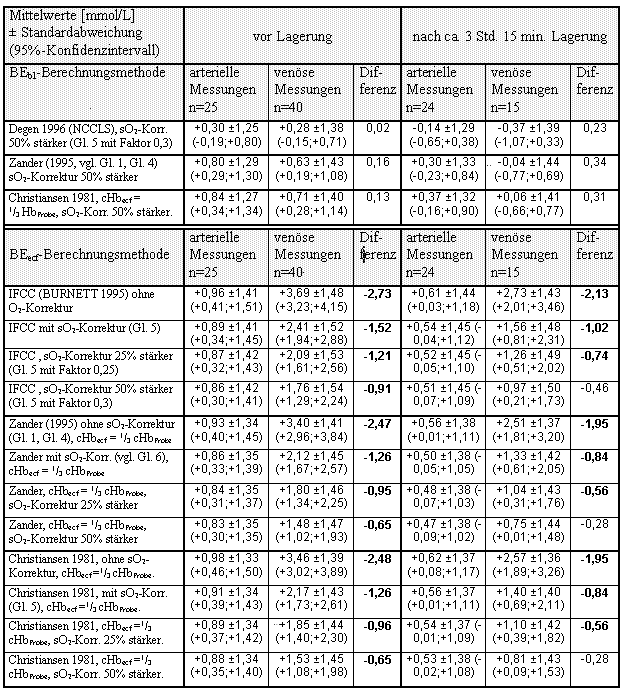
Allerdings mu▀ kritisch angemerkt werden, da▀ es sich hierbei um Blutproben nur eines Probanden handelt. Trotzdem wird durch diese Messungen die bereits aus den Me▀ergebnissen an Patientenblut abgeleitete These gest³tzt, da▀ der von ZANDER (1995) vorgeschlagene Korrekturfaktor zum Ausgleich der arterio-ven÷sen BEecf-Differenz zu niedrig gewõhlt ist.
Einflu▀ des Tonometrierens auf die Basenabweichung
F³r einen Teil der
durchgef³hrte Messungen wurde Blut verwendet, das zuvor im
Tonometer IL 237 mit bekannten Gaspartialdr³cken einheitlich 15 Minuten bei
37░C õquilibriert worden war. In den Lungen ben÷tigt der Gasaustausch hingegen
physiologisch etwa 0,3 s m÷glich [THEWS, 1990], also ca. 1/2000 der zum
Tonometrieren ben÷tigten Zeit. Wõhrend des Tonometrierens fiel bei vorliegenden
Messungen der unter Ber³cksichtigung der sO2 errechnete BEbl
um durchschnittlich ¢2,17 mmol/L ab (vgl. Tabelle 19). Es fõllt jedoch
auf, da▀ der BE-Abfall der tonometrierten Blutproben im Vergleich zur ven÷sen
Ausgangsmessung im Verlauf beider Serien kontinuierlich geringer wird, obwohl
sich die Reihenfolge der Gase unterschied. Dies macht einen prõanalytischen
Fehler plausibel. Von Lagerungseffekten wõre jedoch ein Abfall, und nicht wie
vorliegend beobachtet ein Anstieg des BE zu erwarten. Wie an den ven÷sen und
arteriellen Kontrollmessungen festgestellt werden konnte, waren die
BE-Verõnderungen durch Lagerung in Eiswasser gering (vgl. auch M▄LLER-PLATHE,
1982).
Der geringere BE-Abfall nach Gerõteangaben am zweiten im Vergleich zum ersten Tag ist offenbar durch die h÷here Sauerstoffsõttigung des ven÷sen Blutes in der zweiten Serie bedingt. Bei einheitlicher Berechnung unter Ber³cksichtigung der Sauerstoffsõttigung (Gleichung 6), betrõgt der mittlere BE-Unterschied zwischen den ven÷sen Kontrollmessungen und allen Messungen an tonometriertem Blut an beiden Tagen 2,2 mmol/L. Eine m÷gliche Ursache f³r diesen geringeren BE-Abfall im Verlauf der Tonometermessungen k÷nnte darin liegen, da▀ in Blut, das lõnger gek³hlt gelagert wurde, das Tonometrieren einen geringeren BE-Abfall bewirkt.
Aufgrund der starken und nicht konstanten Senkung des BE durch das Tonometrieren selbst mu▀ dieses f³r Gaspartialdr³cke etablierte Verfahren nach vorliegenden Ergebnissen als nur sehr bedingt geeignet f³r die Untersuchung der Basenabweichung angesehen werden.
Vergleich der sauerstoffreichen mit den sauerstoffarmen Proben
Der Einflu▀ des Haldane-Effekts wird durch Vergleich der mit sauerstofffreiem Gas (Gas 3, vgl. Tabelle 5) tonometrierten Proben mit den anderen Proben deutlich, deren Hõmoglobin fast vollstõndig O2-gesõttigt war (Gase 1, 2 und 4). Der Mittelwert der Gerõteangaben lag beim sauerstofffreien Gas um durchschnittlich 2,76 mmol/L h÷her. Bei Verwendung des KorrekturŁterms f³r die Sauerstoffsõttigung (Gl. 5) wird die BEbl-Differenz fast vollstõndig beseitigt. Eine Aussage, ob in diesem Fall der verwendete Faktor von 0,2 in Gleichung 5 tatsõchlich ausreichend ist, um den Haldane-Effekt zu eliminieren, lõ▀t sich mit vorliegenden in vitro Messungen aufgrund des ³berlagerten Effekts der BE-─nderung wõhrend des TonoŁmetrierens jedoch nicht machen. Es kann auch vermutet werden, da▀ sich der durch das Tonometrieren bewirkte BE-Abfall bei Verwendung von sauerstofffreiem Gas von jenem bei Anwesenheit von Sauerstoff unterscheidet. Dies k÷nnte z. B. ³berpr³ft werden indem zwei Blutproben in unterŁschiedlicher Reihenfolge mit einem O2-reichen und einem O2-armen Gas tonometriert werden.
Falls der von ZANDER (1995) empfohlene Faktor durch Messungen an tonometriertem Blut ermittelt wurde, k÷nnte ein geringerer BE-Abfall beim Tonometrieren mit sauerstoffarmem Gas (z. B. durch verminderten Metabolismus) die Ursache daf³r sein, da▀ dieser Faktor wie vorlieŁgend gezeigt bei Messungen an nativem arteriellen und ven÷sem Blut die BE-UnterŁschiede nicht vollstõndig beseitigt.
Die Messung an sauerstofffrei tonometriertem Blut war mit dem Gerõt Nova Stat Profile Ultra nur f³r die erste bzw. die ersten drei Messungen m÷glich, bei denen noch SauerstoffpartialŁdr³cke von durchschnittlich 5,25 mmHg ausgegeben wurden. Danach gab das Gerõt nur FehlerŁmeldungen aus, bis wieder eine Probe mit h÷herem Sauerstoffpartialdruck zugef³hrt wurde. Bei den anderen Gerõten kam es mit dem sauerstofffreien Gas au▀er einer vergleichsweise hohen BE-Streuung in der ersten Me▀serie zu keinen Auffõlligkeiten; allerdings gab insbesondere AVL einen unrealistisch hohen Restsauerstoff an. Derart niedrige Sauerstoffpartialdr³cke haben zwar f³r Blut keine klinische Relevanz, dennoch geben alle Hersteller in den Handb³chern die pO2-Me▀bereiche ab 0,0 mmHg an (vgl. Tabelle 7).
Bedeutung von Pufferl÷sungen als Qualitõtskontrollmaterial
Aufgrund der vorliegend beobachteten starken BE-Differenzen zwischen verschiedenen Analysatoren und der Drift einzelner Gerõte im zeitlichen Verlauf wõre es w³nschenswert, wenn f³r die klinische Routine L÷sungen zur Qualitõtskontrolle verf³gbar wõren, die einen definierten BE-Wert aufweisen, da kein klinisch f³r Routinelabors praktikables ReferenzŁverfahren f³r die BE-Bestimmung existiert. Auch die Tonometrie als klassisches ReferenzŁverfahren der Blutgasanalytik ist aufwendig und aufgrund des im vorherigen Kapitel besproŁcheŁŁnen deutlichen BE-Abfalls durch das Tonometrieren selbst nur eingeschrõnkt f³r den BE verwendbar. Herk÷mmliches Qualitõtskontrollmaterial f³r die Blutgasanalytik ist zur Kontrolle der BasenabŁweichung nicht befriedigend verwendbar, da die Zielwert-Bereiche f³r pH und pCO2 so gro▀ sind, da▀ sich daraus BE-Zielwert-Bereiche von bis zu 8 mmol/L Spannweite errechnen [ZANDER 1995, 2. Referenz]. Daher wurde am Institut f³r Physiologie und Pathophysiologie der UniŁversitõt Mainz eine L÷sung auf Basis von N-(2-Hydroxyethyl)-Piperazin-NÆ-2-EthanŁsulfonŁsõure (HEPES) entwickelt (hergestellt durch Fa. Bioanalytik, Umkirch / Freiburg), deren pH-Wert sich bei ─nderungen des pCO2 (durch Gasõquilibrierung) und der Basenabweichung (durch Titration) gleich verhalten soll wie Blutplasma. Sie wird als äphysiological Acid Base Controlō, kurz äpABCoō, bezeichnet. Durch Titration mit Salzsõure oder Natronlauge kann eine Basenabweichung der L÷sung eingestellt werden, die auch bei ─nderungen des pCO2 konstant bleibt, was wiederum die Angabe eines engeren BE-Zielbereiches erm÷glicht, da ─nderungen eines der Parameter bei Lagerung oder nach dem ųffnen der Ampulle gegenŁlõufige ─nderungen des anderen Parameters verursachen, so da▀ sich der BE beispielsweise bei Entweichen von Kohlendioxid durch falsche Handhabung nicht wesentlich õndert.
Den f³nf f³r die Messungen an tonometriertem Blut vorliegend verwendeten Analysatoren wurde auf den physiologischen pK eingestellte HEPES-L÷sung (pABCo) mit den Zielwerten f³r den BE von 10 ▒ 2, 0 ▒ 2 und ¢10 ▒2 mmol/L je dreimal nacheinander zur Analyse zugeŁf³hrt. Die Messungen wurŁden 16 Tage vor der ersten Serie der in vitro Messungen bzw. 24 Tage vor der zweiten Serie der MessunŁgen an Patientenblut durchgef³hrt. Die Me▀ergebnisse sind in Tabelle zusammengestellt.
Da die pABCo-Pufferl÷sungen hõmoglobinfrei sind und sich wie Blutplasma verhalten sollen, ist die Unterscheidung zwischen BEbl und BEecf nicht sinnvoll. Aufgrund der unterschiedlichen Algorithmen unterschieden sich die von den Gerõten errechneten Werte jedoch bei Messungen an pABCo um bis zu 2,5 mmol/L (Tabelle). Bei einheitlicher BEecf-Berechnung unter Verwendung eines Drittels der Hõmoglobinkonzentration (also ebenfalls 0 g/dL) unterscheidet sich der BEecf der Pufferl÷sung hingegen nicht vom BEbl (vgl. letztes Spaltenpaar in Tabelle).
Es zeigte sich, da▀ das Gerõt von Radiometer den BEbl bis zu 4,74 und den BEecf bis zu 4,45 mmol/L niedriger als den jeweilige Zielwert angibt (Tabelle). Auch das Gerõt IL 1620 bestimmt BEbl-Werte, die bis zu 2,26 mmol/L unter dem Zielwert und damit au▀erhalb des Zielbereichs liegen. Die BEbl-Ergebnisse aller anderen Gerõte liegen im Zielbereich (Zielwert ▒ 2 mmol/L). Au▀er bei metabolischer Azidose liegen auch die einheitlich aus den pH- und pCO2-Me▀werten des Gerõts von IL berechneten BE-Werte au▀erhalb des Zielbereichs. Bei metabolischer Alkalose ergibt die einheitliche Berechnung auch f³r das Gerõt von Nova Biomedical ein Ergebnis au▀erhalb des Zielbereichs. Trotz des f³r den klinischen Einsatz immer noch unbefriedigend breiten Zielbereichs von 4 mmol/L f³r diese Qualitõtskontrollen, wird dieser also trotzdem nicht zuverlõssig von allen Gerõten getroffen.
Tabelle 27: ĀĀĀĀ Me▀ergebnisse an HEPES-Pufferl÷sung mit physiologischem pK, aufsteigend nach dem BEbl sortiert.
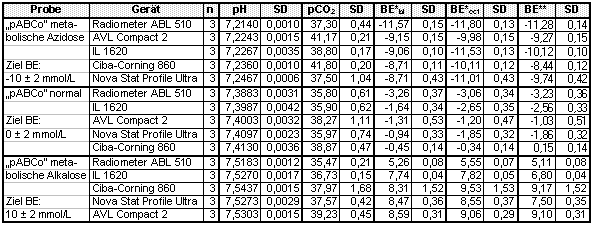
BE*ĀĀĀĀ =ĀĀĀ Mittelwert
der nach der gerõtetypischen Formel errechneten BEbl- (cHb = 0 g/dL)
bzw. BEecf-Werte;
BE**ĀĀĀĀĀĀĀ =ĀĀĀ Mittelwert der nach ZANDER (1995; vgl.
Gleichung 1 und Tabelle 1) mit cHb = 0 g/dL einheitlich
ĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀ berechneten BE Werte.
Die an den pABCo-Pufferl÷sungen gemessenen BE-Werte unterscheiden sich trotz der relativ geringen Anzahl von Messungen zwischen den Analysatoren signifikant (vgl. Tabelle). Die Reihenfolge der nach dem durchschnittlichen BE aufsteigend sortierten Gerõte, ist gegen³ber der in Tabelle 16 f³r Blut ermittelten Sortierreihenfolge v÷llig verschieden. Insbesondere bestimmte das Gerõt von Ciba-Corning bei Blut immer die niedrigsten, an den Pufferl÷sungen hingegen die h÷chsten Basenabweichungen im Gerõtevergleich. Radiometer hatte bei Blut regelmõ▀ig BE-Me▀ergebnisse im Bereich zwischen den anderen Gerõten, ermittelte jedoch an den Pufferl÷sungen Werte, die weit niedriger als die Zielwerte der Kontroll÷sungen und die Resultate der anderen Gerõte waren.
Die mittlere Standardabweichung des pH lag bei diesen Messungen bei 0,0022; bei den Messungen mit Blut an denselben Gerõten (zweite Hõlfte der Messungen mit Patientenblut und die Serien mit tonometriertem Blut) betrug sie 0,0068. F³r den pCO2 lauten die jeweiligen Standardabweichungen 0,568 f³r Pufferl÷sung und 0,931 mmHg f³r Blut. Von normalem Sõure-Basen-Status ausgehend, bewirkt die Addition der Streuung des pH zu dessen Normalwert (7,4) einen BE (nach ZANDER, 1995) von 0,15 (pH = 7,4022, pCO2 = 40 mmHg) bzw. 0,48 mmol/L (pH = 7,4068, pCO2 = 40 mmHg), und die Addition der pCO2 Streuung einen BE von 0,27 (pCO2 = 40,568 mmHg, pH = 7,4) bzw. 0,44 mmol/L (pCO2 = 40,931 mmHg, pH = 7,4). Es wird also deutlich, da▀ die Wiederholungsvariabilitõt der pH Messung bei den Kontroll÷sungen einen geringeren Einflu▀ auf den BE hat als die Variabilitõt des pCO2, wohingegen der Einflu▀ beider Parameter bei den Messungen an Blut etwa gleich war.
Tabelle 28:ĀĀĀĀĀ Darstellung der an allen Analysatoren parallel durchgef³hrten BE-Messungen [mmol/L]. Aufbau der Tabelle und Berechnung der Werte entspricht Tabelle 16. Die Gerõte sind jeweils nach dem Mittelwert der ausgegebenen BEbl-Werte geordnet. Als Ma▀ f³r die Streuung wurde die Standardabweichung der Differenz zwischen den jeweiligen Me▀werten und dem Mittelwert der Parallelmessungen errechnet. Versetzt zwischen den Zeilen der jeweiligen Analysatoren ist die Irrtumswahrscheinlichkeit p bez³glich der Ungleichheit der Verteilungen der Me▀werte (Wilcoxon Vorzeichen-Rang-Test) angegeben.
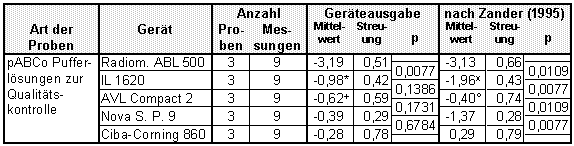
Ergõnzende p-Werte:
* p (IL 1620; Nova Stat Profile 9) = 0,0109ĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀ + p (AVL Compact 2;Ciba-Corning 860) = 0,3139
x p (IL 1620; Nova Stat Profile 9) = 0,0109ĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀ ░ p (AVL Compact 2;Ciba-Corning 860) = 0,0663
Der gr÷▀te Unterschied zwischen den durchschnittlichen pH-Werten eines Gerõts lag bei 0,0238 f³r Messungen an pABCo-Kontroll÷sung (Radiometer ¢ Ciba-Corning; vgl. Tabelle Āb), f³r die Messungen mit Patientenblut betrug er bei 0,0378 (Ciba-Corning ¢ Nova; vgl. Tabelle Āb, Serie 2). Also unterscheiden sich die Gerõte bei der pH-Bestimmung an Pufferl÷sung weniger stark als an Blut, was dadurch begr³ndet werden kann, da▀ die automatische Kalibrierung der Gerõte ebenfalls mit HEPES-Pufferl÷sung durchgef³hrt wird. Beim Vergleich von f³nf anderen Blutgasanalysatoren stellten DEVGUN et al. (1983) eine etwa doppelt so gro▀e (0,047) durchschnittliche pH-Differenz zwischen den zwei sich am meisten unterscheidenden Gerõten bei Messungen von Kontroll÷sungen fest.
F³r den pCO2 betrug die maximale Differenz zwischen den Mittelwerten 3,37 mmHg (Radiometer ¢ AVL) bei pABCo-Messungen, 1,53 mmHg f³r Patientenblut (IL ¢ AVL) und 2,24 mmHg in den Tonometer-Me▀serien. Obwohl die Kohlendioxidpartialdr³cke bei Messungen an pABCo eine um etwa 1/3 bessere Wiederholungsgenauigkeit haben (vgl. Spalte äStreuungō in Tabelle ), unterscheiden sich die Gerõte untereinander also deutlich stõrker als bei Messungen an Blut. DEVGUN et al. (1983) ermittelten bei Kontroll÷sungen eine mittlere pCO2-Differenz zwischen zwei aus f³nf Gerõten von maximal 2,17 mmHg. VAN KESSEL et al. (1987) ermittelten eine Differenz zwischen zwei aus 10 Gerõten (9 Modelle, 4 Hersteller) von maximal 3,3 mmHg bei einem Zielwert von 20 mmHg und von maximal 6,4 mmHg bei einem Zielwert von 70 mmHg an tonometriertem Blut, wobei die Differenzen offenbar mehr vom einzelnen Gerõt als vom Hersteller abhõngig sind. Auch die Standardabweichungen lagen etwa im Bereich der vorliegend festgestellten, wobei allerdings die maximalen Standardabweichungen bei etwa 2 mmHg lagen. Es befanden sich keine Gerõte von Nova Biomedical oder AVL unter den Testgerõten.
Insgesamt scheinen also die vorliegend beobachteten Unterschiede zwischen den Analysatoren bei pH- und pCO2-Messungen f³r heute verbreitete Analysatoren ³blich zu sein.
Tabelle 29 a und b:
Darstellung der an allen Analysatoren parallel durchgef³hrten pCO2- (a) und pH-Messungen (b) an HEPES-L÷sung (äpABCoō). Die der Aufbau dieser Tabelle entspricht Tabelle .
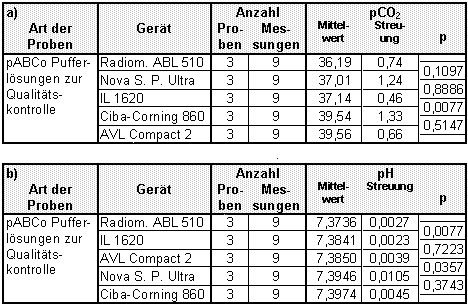
Wie aus Tabelle Āim Vergleich mit Tabelle Āersichtlich ist, unterschied sich sowohl beim pCO2 als auch beim pH das Verhõltnis der Ergebnisse zwischen den Messungen an Pufferl÷sung und den Messungen an Blut signifikant voneinander. Beispielsweise ermittelte das Gerõt Nova Stat Profile Ultra bei pCO2-Messungen sowohl mit Patientenblut als auch mit tonometriertem Blut (vgl. Tabelle ) signifikant h÷here Kohlendioxidpartialdr³cke als das Gerõt von Ciba-Corning; bei den Messungen an Kontrolll÷sungen waren sie hingegen bei allen drei untersuchten pABCo-Arten (vgl. Tabelle) und insgesamt signifikant niedriger (vgl. Tabelle ). Bez³glich des pH hat das Gerõt von Ciba-Corning bei Messungen mit pABCo signifikant h÷here Werte als alle anderen Gerõte au▀er jenem von Nova, wohingegen es mit Blut in allen Me▀serien die niedrigsten Werte ermittelt. Auch das Gerõt von IL ermittelte an pABCo signifikant h÷here Werte als jenes von Radiometer. Mit Blut wurden hingegen durch das Gerõt IL 1620 bei den im selben Monat durchgef³hrten Messungen signifikant niedrigere Werte festgestellt.
Es darf also nicht unkritisch angenommen werden, da▀ eine ▄bereinstimmung zwischen Me▀wert und Zielwert bei einer Qualitõtskontrolle auch valide Messungen an Blut garantiert. Die je nach Analysator unterschiedlichen Zielbereiche, die bei kommerziell vertriebenen Qualitõtskontrollmaterialien angegeben werden, haben vermutlich die Aufgabe, gerõtebedingte Unterschiede zwischen Messungen in diesen Pufferl÷sungen und Messungen in Blut auszugleichen. Allerdings ist fraglich, ob bei Bestimmung der Zielbereiche tatsõchlich nur gerõtetypspezifische Unterschiede (Aufbau der Elektroden, Zusammensetzung von Pufferl÷sungen in den Elektroden) ber³cksichtigt wurden, oder ob auch zeitweilige (wie z.B. der vorliegend beobachtete pH-Drift beim Gerõt von AVL) oder durch Eigenheiten des speziellen Exemplars bedingte Unterschiede (wie z.B. vorliegend bei der pCO2-Bestimmung durch die beiden Nova-Gerõte) ma▀geblich in die Zielwertfestlegung eingingen. Da die Hersteller von Gerõten auch Kontrollmaterialien anbieten, f³r die auch Zielbereiche f³r eine willk³rlich erscheinende Auswahl von Gerõten der Konkurrenzunternehmen angegeben sind, wõre es vorstellbar, da▀ diese Zielbereiche an wenigen oder sogar jeweils nur einem Exemplar einer Gerõtegrupp mit gleicher Me▀vorrichtung bestimmt wurden.
Die Auswertung der Daten der Messungen an Fluorocarbon-Qualitõtskontroll÷sungen durch ³ber 900 bei der American Thoracic Society registrierte Analysatoren [HANSEN et al., 1998] zeigŁte systematische Fehler zwischen den Gerõten verschiedener Hersteller, die weder mit den vorŁliegend f³r Blut noch f³r Qualitõtskontrolll÷sungen festgestellten ³bereinstimmten. Die maxiŁmalen Unterschiede zwischen dem Mittelwert aller Messungen der Gerõten verschiedener Hersteller (Ergebnisse von Analysatoren der Firma Nova Biomedical wurden nicht publiziert) lagen dabei f³r den pCO2 bei bis zu 4 mmHg bei 40 mmHg (AVL > Radiometer) und f³r den pH bei knapp 0,04 im pH-Bereich 7,3 bis 7,4; dies stimmt etwa mit den vorliegenden Ergebnissen ³berein.
Methodenkritik
In dieser Studie wurden nur beatmete Patienten in stabilem klinischem Zustand aufgenommen, die alle einen ausgeglichenen Sõure-Basen-Haushalt oder eine mõ▀ige metabolische Azidose aufwiesen. Aus Tabelle ist ersichtlich, da▀ die ven÷sen Proben bei kritischeren klinischen Bildern einen relativ niedrigeren BEecf aufweisen. Bei Betrachtung des BEbl anstelle des BEecf wird die arterio-ven÷se Differenz ebenfalls gr÷▀er; dies ist darauf zur³ckzuf³hren, da▀ bei hohen Kohlendioxidpartialdr³cken (z. B. in ven÷sem Blut) BEbl-Werte niedriger als BEecf-Werte sind, sich bei Normokapnie jedoch weitgehend entsprechen. Sofern niedrige Hõmoglobinkonzentrationen in die Gleichungen eingesetzt werden, õhnelt der BEbl hingegen eher dem BEecf, wodurch auch die arterio-ven÷se Differenz kleiner wird (vgl. Abbildung 2).
Alle Proben wurden den Patienten aus Verweilkathetern und den Probanden durch direkte Punktion entnommen. Von RISCH et al. (1999) wurde ein signifikanter pO2-Unterschied zwischen durch direkte Punktion gewonnenen Proben und solchen aus Verweilkathetern bei Sauerstoffpartialdr³cken von durchschnittlich etwa 500 mmHg ermittelt. F³r die anderen Parameter der Blutgasanalytik liegen keine Untersuchungen vor, es ist jedoch von bedeutend geringeren Unterschieden auszugehen, wie sich aus Studien zur Ermittlung der Gasdiffusion durch Kunststoffspritzen vermuten lõ▀t [M▄LLER-PLATHE et al., 1992].
Zum Vergleich zwischen arteriellen und kapillaren Messungen des Sõure-Basen-Status wurden bereits viele Studien durchgef³hrt, die zwar z. B. bei Patienten im Schockzustand bedeutende Unterschiede des pH und pCO2 aufzeigten, jedoch nicht bez³glich des BE [SIGGAARD-ANDERSEN 1968]. OÆSULLIVAN (1971) schlo▀ aus eigenen Messungen, da▀ bez³glich des Sõure-Basen-Haushaltes auch peripherven÷se Proben v÷llig angemessen sind, selbst bei Patienten im Schockzustand; dies steht im Widerspruch zu PHILLIPS et al. (1969).
Leider mu▀te vorliegend auch ungeklõrt bleiben, warum bei f³nf der zwanzig Patienten gro▀e arterio-ven÷se Differenzen sowohl in den Blutgas-Me▀werten als auch in anderen Parametern bestanden. Daraus lõ▀t sich zumindest die Forderung ableiten, bei Probenentnahme zu kontrollieren, da▀ es sich tatsõchlich um reprõsentative Proben des Patienten handelt. Zu diesem Zweck k÷nnen wie vorliegend Parameter ohne relevanten Einflu▀ auf pH und pCO2 verglichen werden. Aus diesem Grund ist eine Bestimmung der Hõmoglobinkonzentration in den Analysatoren sinnvoll, obwohl die hier festgestellte Me▀genauigkeit f³r den regulõren klinischen Einsatz noch nicht ausreichend ist.
Der Haldane-Effekt konnte zwar auch bei vorliegenden in vitro Messungen deutlich aufgezeigt werden, aufgrund der starken Verõnderung des BE durch den Vorgang des Tonometrierens war jedoch eine zuverlõssige Qualifizierung nicht m÷glich.
Tabelle 30: ĀĀĀĀ Darstellung der aus den Mittelwerten von pH, pCO2 und pO2 errechneten arterio-ven÷sen BE-Differenzen [mmol/L] aus drei verschiedenen Studien. Zum Vergleich sind die Ergebnisse der vorliegenden Patientenme▀reihen ebenfalls dargestellt.
ĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀ Die drittletzte Spalte wurde nach Gleichung 6 berechnet; in der viertletzten Spalte wurde der Faktor des sO2-Ausgleichsterms aus Gleichung 6 auf 0,3 mmol/L pro g Hb erh÷ht. Die beiden letzten Spalten entsprechen den in den Gerõten von Radiometer verwendeten Gleichungen f³r SBE (BEecf) und ABE (BEbl) und entsprechen weitgehend dem Nomogramm von SIGGAARD-ANDERSEN und ENGEL (1960).
ĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀĀ Aus der Tabelle ist ersichtlich, da▀ bei verschiedenen pathologischen Zustõnden der ven÷se BE deutlich niedriger als der arterielle sein kann, und da▀ die Berechnung des BEbl relativ niedrige ven÷se Werte ergibt, so da▀ bei diesem errechneten Wert die Ber³cksichtigung des Haldane-Effekts nicht notwendig erscheint.
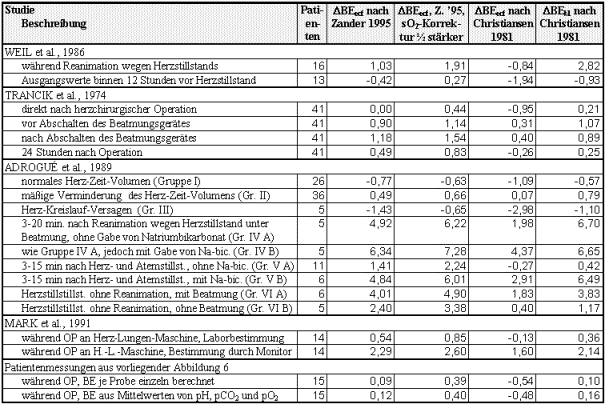
Anmerkungen: Da die BE-Berechnung aus Mittelwerten der Eingangsvariablen mathematisch nicht korrekt ist, aber aufgrund der Mittelwertbildung in den Tabellen der verwendeten Studien nicht vermeidbar war, wurde bei den eigenen Daten der BE sowohl f³r jede Probe einzeln berechnet (vgl. Tab. 18) als auch aus den Mittelwerten berechnet (letzte beiden Zeilen). Die gen³gende Zuverlõssigkeit dieses Berechnungsverfahrens konnte auch dadurch bestõtigt werden, da▀ sich bei den Tonometermessungen ebenfalls keine bedeutenden Differenzen zwischen diesen beiden Arten der Mittelwertbildung ergaben (maximal 0,047 mmol/L).
Da in diesen Vergleichsstudien die Hõmoglobinkonzentrationen der Proben nicht erwõhnt wurden, wurde einheitlich vom Standardwert 15 g/dL ausgegangen. Dies erscheint bei teilweise multiŁmorŁbiden Patientenkollektiven hoch, wurde jedoch in der einzigen dieser Studien, die BE-Werte angibt [TRANCIK et al., 1974], offenbar ebenfalls getan. Bei der BE-Berechnung aus den Werten von WEIL et al. (1986) mu▀te von einem arteriellen pO2 von 100 mmHg und einem ven÷sen pO2 von 30 mmHg (in Anlehnung an die Werte von ADROGU╔) ausgegangen werden, da keine Werte angegeben wurden.
Schlu▀betrachtung und Ausblick
Argumente f³r die Ber³cksichtigung der Sauerstoffsõttigung bei der BEecf-Bestimmung
Gegenwõrtig ersetzt der BEecf zunehmend den klassischen in vitro BEbl. Vorliegend konnte gezeigt werden, da▀ bei Verwendung des BEecf die Ber³cksichtigung der Sauerstoffsõttigung noch notwendiger ist als bei Verwendung des BEbl, f³r den sie bisher nur empfohlen wurde, ohne da▀ sie sich bei den Gerõteherstellern, in der klinischen Routine und in allen Bereichen der Forschung durchsetzen konnte. Die wahrscheinliche Ursache daf³r besteht darin, da▀ ven÷se BEbl-Werte hõufig niedriger als arterielle sind, obwohl aufgrund des seit ³ber 80 Jahren bekannten Haldane-Effekts das Gegenteil zu erwarten wõre. Diese ä▄berraschungō [TRANCIK et al., 1974] ist jedoch, wie vorliegend gezeigt, ein Artefakt aufgrund der Annahme einer vorgegebenen Hõmoglobinkonzentration von zumeist 15 g/dL, obwohl die wirksame HõmoŁglobinkonzentration in dem Fl³ssigkeitskompartiment, dessen Sõure-Basen-Status tatsõchlich gemessen und therapiert wird, bei den meisten Patienten sogar weniger als 5 g/dL betrõgt (Ausgleich von Blut mit dem gr÷▀eren interstitiellen Fl³ssigkeitsraum und Hõufigkeit von Anõmien insbesondere bei õlteren und multimorbiden Patienten). Wenn eine entsprechende Hõmoglobinkonzentration bei der Berechnung zugrunde gelegt wird, also der BEecf berechnet wird, ist von einem relativen Anstieg des ven÷sen BEecf auszugehen, der korrigiert werden sollte. Die vorliegend durchgef³hrte sO2-Korrektur des BEecf lõ▀t sich ohne produktionstechnischen Mehraufwand in moderne Blutgasanalysatoren integrieren. Bei arteriellen oder kapillaren Proben f³hrt sie bei befriedigender Oxygenierung zu keiner ─nderung der Ergebnisse; bei ven÷sen Proben f³hrt sie hingegen zu einer deutlich besseren Vergleichbarkeit. Es ist zu vermuten, da▀ die sO2-Korrektur auch bei schlechter Lungenfunktion eine bessere Voraussage der zu erwartenden Effekte einer ausreichenden Beatmung auf den Sõure-Basen-Status erm÷glicht.
Die aus Messungen von ADROGU╔ et al. (1989), MARK et al. (1991), TRANCIK et al. (1974) und WEIL et al. (1986) vorliegend ermittelte stõrkere ven÷se als arterielle BEecf-Senkung bei kritisch Kranken (vgl. Tabelle) hat m÷glicherweise eigenstõndige diagnostische Bedeutung, was Thema weiterer Untersuchungen ist.Ā
Beispielrechung zur Fehleraddition
Die Summe der in der Blutgasanalytik bestehenden Fehlerm÷glichkeiten ist wie vorliegend gezeigt immer noch betrõchtlich. Dies zeigt sich bei der Berechnung der Basenabweichung besonders deutlich, da sich in diesem Wert Me▀fehler bei der Bestimmung von pH und pCO2 gegenseitig verstõrken k÷nnen und zusõtzlich durch die Berechnung bedingte Unterschiede bestehen. Systematische Fehler zwischen den Gerõten k÷nnen im ung³nstigen Fall auf etwa 5 mmol/L quantifiziert werden. Ausrei▀er bei Einzelmessungen von ³ber 6 mmol/L wurden beobachtet. Falls zu diesen Fehlern noch BE-Formelunterschiede von 4 mmol/L und ein Fehler durch Nichtbeachtung der Sauerstoffsõttigung bei einer ven÷sen Probe von 2 mmol/L hinzukõmen, k÷nnte bei sehr ung³nstiger Addition der Fehler ohne jegliche prõanalytische Fehler ein Gesamtfehler von 17 mmol/L entstehen, also z.B. bei einem Patienten mit v÷llig normalem Sõure-Basen-Status irrt³mlich eine schwere metabolische Alkalose ermittelt werden.
Gr³nde f³r die Notwendigkeit einer weiteren Verbesserung der Me▀genauigkeit
Aus einer StandardŁabweichung bei Paarmessungen von 0,40 mmol/L und der intra-individuellen Varianz wurde von HARDING und FRASER (1987) errechnet, da▀ zwei BE-Werte mindestens 3,3 mmol/L auseinander liegen m³ssen, um als signifikant verŁschieŁden gelten zu k÷nnen. Dies wurde als Argument daf³r gesehen, da▀ der klinische Gebrauch dieses abgeleiteten Parameters insgesamt verwirrend sein k÷nnte. Die durchschnittliche Standardabweichung bei Wiederholungsmessungen betrug vorliegend 0,49 mmol/L (Mittelwert der BE-Streuungswerte aus Tabelle 14). Da die Basenabweichung jedoch ein gro▀es diagnostisches Potential bietet, ist eine weitere Steigerung der Me▀g³te anzustreben. Dabei sind insbesondere die Hersteller der Gerõte gefordert. Wie aus den Unterschieden zwischen den Gerõten ersichtlich ist (vgl. Tabelle), besteht auf dem Gebiet der Prõzisionsverbesserung und der Fehlerdetektion durch die Analysatoren noch in unterschiedlichem Ma▀e Verbesserungspotential. Auch die Langzeitkonstanz (z.B. von Kalibrationspuffern und Elektroden) sollte noch wesentlich verbessert werden, und die Analysatoren sollten Instabilitõten der Me▀einŁrichtungen zuverlõssiger feststellen. Damit die M÷glichkeit besteht, Fehlfunktionen der Gerõte aufzuŁdecken, werden Kontrollmaterialien ben÷tigt, die eine zuverlõssige Aussage dar³ber zulassen, wie genau ein Gerõt die entsprechenden Parameter an Blut bestimmen kann. Untersuchungen, ob gegenwõrtig verbreitete Qualitõtskontrollen diese Forderung besser erf³llen als die vorliegend vorgestellte pABCo-L÷sung liegen allerdings noch nicht vor. F³r die Gaspartialdr³cke bleibt die Gasõquilibrierung von Frischblut vorerst weiter das Referenzverfahren der Wahl. Leider existiert f³r den pH kein vergleichbares Referenzverfahren. Die zur Kalibration oder Qualitõtskontrolle verwendeten Pufferl÷sungen haben den Nachteil, da▀ auch Unterschiede in ihrer Zusammensetzung das Membranpotential an der pH-Elektrode beeinflussen k÷nnen, was vermutlich die Ursache f³r die vorliegend beobachtete mangelhafte Vergleichbarkeit von Messungen an Blut mit solchen an Pufferl÷sung ist. Idealerweise ist jedoch von einem Anaysator eine weitgehende Unempfindlichkeit gegen derartige Einfl³sse der Probenzusammensetzung zu fordern, insbesondere da die Gerõte auch andere K÷rperfl³ssigkeiten (z.B. Urin oder Magensaft) und Atemgase analysieren k÷nnen sollten. Vorliegend konnte auch gezeigt werden, da▀ die Wiederholungsgenauigkeit der pH-Messung in Blut von Patienten wõhrend Operationen signifikant schlechter war als in Blut gesunder Probanden; auch dies sollte bei Untersuchungen der Gerõteprõzision ber³cksichtigt werden.
Trotz der theoretischen Einwõnde gegen regelmõ▀ige zentral gesteuerte Qualitõtskontrollen sollten auch in Deutschland Ringtests an allen im klinischen Einsatz befindlichen Analysatoren durchgef³hrt werden. Die bei zwei Ringtests in ųsterreich verwendeten Zielbereiche [WITEK, 1978] von ▒5% f³r den pCO2 und ▒0,2% f³r den pH erscheinen jedoch im Hinblick auf den BE als zu gro▀. Eine pCO2-Erh÷hung um 5% und eine pH-Erh÷hung um 0,2% entspricht einer BE-Steigerung um 2 mmol/L bei Normalbedingungen, bei mõ▀iger Alkalose jedoch um bereits ³ber 3 mmol/L (10 auf 13 mmol/L). Jedoch wurde auch dieser weite Zielbereich bei diesen Ringtests nur bei etwa der Hõlfte der Messungen erreicht, was als noch befriedigendes Ergebnis bezeichnet wurde. Diese Auffassung ist bei isolierter Betrachtung von pH und pCO2 nachvollziehbar, f³r die Berechnung des BE sind diese Streuungen nach vorliegenden Ergebnissen jedoch zu gro▀.
Die von drei der untersuchten Gerõte ermittelten Hõmoglobinkonzentrationen wiesen eine f³r den klinischen Einsatz zu hohe Streuung auf, so da▀ die Bestimmung dieses Parameters noch erheblich verbessert werden mu▀, um z. B. Blutverluste wõhrend Operationen ausreichend zuverlõssig feststellen zu k÷nnen. Prinzipiell sind Gerõte, die m÷glichst viele sogenannte äNotfallparameterō automatisch bestimmen zwar im Sinne der Arbeitserleichterung und der Beschleunigung der Diagnosestellung zu begr³▀en, jedoch mu▀ jeder dieser Parameter in praxisnahen Studien gepr³ft werden. Wie sich vorliegend am Beispiel der cHb zeigte, gen³gen gute Me▀ergebnisse am Blut gesunder Probanden nicht.
Ma▀nahmen zur Vermeidung von Me▀fehlern
Zur Vermeidung von Fehlern bei der BEecf-Bestimmung sollten nach den hier erhobenen Befunden folgende Punkte beachtet werden:
Prõanalytisch
Ę Bei der Blutprobe mu▀ es sich um f³r den Patienten insgesamt reprõsentatives Blut handeln. Es mu▀ sichergestellt werden, da▀ sich im Entnahmekatheter keine Reste von Infusions- oder Antikoagulationsl÷sungen mehr befinden. Die Antikoagulation sollte mit einer geringen, gleichbleibenden Menge Heparin erfolgen, z. B. bei VerwendungĀ von herstellerseitig nicht heparinisierten Einmalspritzen durch Verteilung von Natrium-Heparinl÷sung mit 5 000 I.E./mL an der Spritzenwand und durch die nach Entleerung der Spritze im Totraum verbleibende Heparinmenge.
Ę Die Probe soll m÷glichst ohne Luftkontakt entnommen werden. (Dieser Punkt ist vor allem f³r den Sauerstoffpartialdruck wichtig.)
Ę Wenn ein Transport oder eine Lagerung der Proben nicht vermeidbar ist, sollte dies gek³hlt (z. B. in Styroporbox mit Eiswasser) erfolgen, da bei ungek³hlter Lagerung bereits nach wenigen Minuten mit einem nur ungenau voraussagbaren BE-Abfall zu rechnen ist.
Ę Die Probe soll vor der Analyse gut durchmischt werden.
Ę Bei Analysatoren mit Probeneinspritzung (z. B. Radiometer ABL 500 / 510, AVL Compact 2) soll mindestens der Inhalt des Spritzenkonus unmittelbar vor der Analyse in einen Tupfer verworfen werden.
Ę Insbesondere Personen mit relativ wenig Erfahrung in Probenentnahme und Analyse sollten ihre Ergebnisse auch bei geringem Verdacht auf methodische Fehler kritisch ³berpr³fen, z. B. durch erneute Messung. Eventuelle Unregelmõ▀igkeiten bei Entnahme oder Analyse sollen entsprechend vermerkt und weitergeleitet werden. Bekannterma▀en unsichere Ergebnisse sind selten Ursache f³r unangemessene Therapie und k÷nnen nachgefordert werden, falls dies im klinischen Gesamtbild notwendig erscheint; das Ignorieren von Besonderheiten bei Abnahme oder Analyse kann hingegen zu bedeutenden Fehleinschõtzungen f³hren [WUILLEMIN et al., 1995].
Kontrolle der Gerõte (intraanalytisch)
Da Instabilitõten von Elektroden offensichtlich von den Gerõten selbst noch nicht zuverlõssig erkannt werden, mu▀ die Stabilitõt der Messungen durch gelegentliche Mehrfachbestimmungen ³berpr³ft werden. Bedeutende Abweichungen zwischen Messungen an derselben Probe sollten den Reprõsentanten der Gerõtehersteller umgehend mitgeteilt werden. Die Ausdrucke von Doppelbestimmungen stellen einfach erklõrbare Dokumente bei eventuellen Reklamationen dar.
Konstante Abweichungen der Me▀werte (äbiasō) sind schwerer aufzudecken, insbesondere wenn in einem Labor nur ein Gerõt oder ein Typ von Blutgasanalysatoren vorhanden ist. Allerdings zeigte sich bei vorliegenden Messungen, da▀ derartige Abweichungen zwischen Analysatoren ³ber 4 mmol/L betragen k÷nnen, und damit klinisch sehr relevant sind. Generell mu▀ aufgrund des Fehlens eines universellen und ³berpr³fbaren Standards in der BE-Bestimmung jedes Labor einen eigenen Referenzbereich festlegen und dessen Einhaltung kontinuierlich ³berpr³fen. Wenn mehrere Blutgasanalysatoren verf³gbar sind, sollten tõglich einige Proben direkt nacheinander an verschiedenen Gerõten analysiert werden. Zufõllige, normalverteilte Fehler k÷nnen durch Doppelbestimmungen reduziert werden (um den Faktor 2 ¢0,5); ebenso kann eine kritische Zunahme intraanalytischer Fehler durch DoppelbeŁstimŁmungen festgestellt werden. Dies kann als Argument f³r eine generelle Doppelbestimmung bei Blutgasanalysen gelten [METZGER et al., 1987], zumindest sollten jedoch klinisch besonders bedeutende Proben mehrfach bestimmt werden.
Um Me▀fehler erkennen zu k÷nnen, sollten Verlaufsmessungen zuverlõssig als solche erkannt werden und wenn m÷glich am selben Gerõt durchgef³hrt werden. Es sollte klar geregelt sein, wie bei Verdacht auf einen Me▀fehler zu verfahren ist. Wenn ein Arzt Zweifel an der Richtigkeit eines Laborwerts hat, sollte er dies umgehend einer zustõndigen Stelle melden. In diesem Zusammenhang ist es positiv zu werten, da▀ moderne Analysatoren viele Parameter en bloc messen, wie die vorliegend untersuchten Gerõte Nova Stat Profile Ultra und Ciba-Corning 860, da auf diese Weise ohne deutlichen Mehraufwand Parameter regelmõ▀ig gemessen werden, bei denen unerwartete Werte Anla▀ zur ▄berpr³fung des Gerõtes geben k÷nnen.
Berechnungsunterschiede (postanalytisch)
Eine einheitliche Berechnung wõre f³r den BEecf ebenso wie f³r den BEbl (solange er noch verwendet wird) und das Bikarbonat sehr w³nschenswert. Von Fachgesellschaften und Herstellern ist daher eine rasche Einigung zu fordern. Bis dahin kann nur empfohlen werden, die klinikinternen Referenzbereiche entsprechend anzupassen. Allerdings zeigen sich die gr÷▀ten Abweichungen zwischen den Formeln bei pathologischen WerteŁkonŁstellationen, die au▀erhalb der Referenzbereiche liegen. Wenn verschiedene Analysatoren verwendet werden, sollte aus den Berichten klar erkennbar sein, um welches Gerõt es sich handelt, und Verlaufskontrollen sollten nur auf einem der Gerõte durchŁgef³hrt werden. Elektronische Datenverarbeitungssysteme sollten die Werte einŁheitŁlich unter Verwendung eines modernen Algorithmus errechnen und nicht von den angeschlossenen Analysatoren direkt ³bernehmen. Wenn eine Formel im Zuge der Vereinheitlichung geõndert wird, sollte dies allen ─rzten mitgeteilt werden, m÷glichst mit einer Grafik, aus der die Unterschiede zu den bisherigen Werten klar hervorgehen.
Wenn die Berechnungsmethode umgestellt wird, kann auch Abbildung 4 herangezogen werden, um sich einen ▄berblick ³ber die Unterschiede zwischen den Formeln zu verschaffen. W³rde beispielsweise die NCCLS-Formel von 1982 (vorliegend von Nova Biomedical und IL verwendet) durch die aktuelle NCCLS-Empfehlung ersetzt (vorliegend von Ciba-Corning verwendet), so w³rde dies au▀er bei ausgeprõgter metabolischer Azidose, bei der sich die Formeln praktisch nicht unterscheiden, zu einer Abnahme der BE-Werte f³hren, die bei Normalwerten (pH = 7,4; pCO2 = 40 mmHg) etwa 0,6 mmol/L betrõgt, bei metabolischer Alkalose jedoch kontinuierlich ansteigt, so da▀ grob angenommen werden kann, da▀ ein BEecf von 12 mmol/L einem BEecf von 13 mmol/L vor der Umstellung entsprechen w³rde.
Obwohl bisher nicht in der Literatur beschrieben, ist nach vorliegenden Ergebnissen eine Anpassung des BEecf an die Sauerstoffsõttigung sinnvoll, insbesondere wenn gelegentlich ven÷se Blutgasanalysen durchgef³hrt werden oder bei hypoxischen Patienten. Allerdings zeigte sich auch, da▀ mit dem von ZANDER (1995) vorgeschlagenen Faktor (Gleichung 5) der Haldane-Effekt nur zu etwa 2/3 kompensiert wird, so da▀ der schon 1937 [DILL et al.] ermittelte Faktor von 0,03 mmol/L je Gramm Hõmoglobin als immer noch g³ltig angesehen werden kann.